题目内容
四个试剂瓶中分别盛装有NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,请就如何检验出这四种溶液回答下列各题.在四支试管中分别取四种溶液各1mL,做下列实验:
(1)在四支试管中分别滴入 (选填稀盐酸或稀硝酸),出现气泡的是 ,离子方程式是 .
(2)在剩余三支试管中分别滴入 ,出现白色沉淀的是 ,离子方程式是 .
(3)在剩余两支试管中分别滴入 ,出现白色沉淀的是 .三次实验中都没有明显现象的是 .
(1)在四支试管中分别滴入
(2)在剩余三支试管中分别滴入
(3)在剩余两支试管中分别滴入
考点:物质的检验和鉴别的实验方案设计,离子方程式的书写
专题:离子反应专题
分析:NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,加盐酸检验碳酸钠会干扰NaCl检验,则加硝酸检验碳酸钠,剩余三种物质中与硝酸钡反应生成沉淀的为Na2SO4溶液,最后对剩余的两种物质中与硝酸银反应生成白色沉淀的为NaCl,则另一无现象的为NaNO3溶液,以此来解答.
解答:
解:(1)加盐酸检验碳酸钠会干扰NaCl检验,则加稀硝酸检验碳酸钠,即出现气泡的为Na2CO3溶液,发生的离子反应为CO32-+2H+=H2O+CO2↑,
故答案为:稀硝酸;Na2CO3溶液;CO32-+2H+=H2O+CO2↑;
(2)剩余三支试管中分别滴入Ba(NO3)2溶液,出现白色沉淀的是Na2SO4溶液,发生的离子反应为Ba2++SO42-=BaSO4↓,
故答案为:Ba(NO3)2溶液;Na2SO4溶液;Ba2++SO42-=BaSO4↓;
(3)剩余两支试管中分别滴入AgNO3溶液,出现白色沉淀的是NaCl溶液,而三次实验中都没有明显现象的是NaNO3溶液,故答案为:AgNO3溶液;NaCl溶液;NaNO3溶液.
故答案为:稀硝酸;Na2CO3溶液;CO32-+2H+=H2O+CO2↑;
(2)剩余三支试管中分别滴入Ba(NO3)2溶液,出现白色沉淀的是Na2SO4溶液,发生的离子反应为Ba2++SO42-=BaSO4↓,
故答案为:Ba(NO3)2溶液;Na2SO4溶液;Ba2++SO42-=BaSO4↓;
(3)剩余两支试管中分别滴入AgNO3溶液,出现白色沉淀的是NaCl溶液,而三次实验中都没有明显现象的是NaNO3溶液,故答案为:AgNO3溶液;NaCl溶液;NaNO3溶液.
点评:本题考查物质的检验实验方案的设计,为高频考点,把握物质的性质及检验时发生的反应、现象为解答的关键,注意检验物质中不能引入干扰离子,题目难度不大.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
下列原子团中,属于羟基的是( )
| A、-NO2 |
| B、-OH |
| C、-COOH |
| D、OH- |
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法错误的是( )


| A、试剂1可以选用石灰乳 |
| B、从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2═2Cl-+Br2 |
| C、工业上,电解熔融MgO冶炼金属镁可减小能耗 |
| D、可用BaCl2溶液除去粗盐中的SO42- |
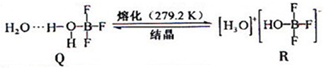
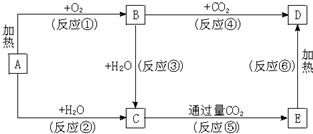
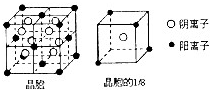 A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大.B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族.B、C、D的最高价氧化物的水化物均能互相反应生成盐和水,D的原子半径是同周期原子中最小的.
A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大.B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族.B、C、D的最高价氧化物的水化物均能互相反应生成盐和水,D的原子半径是同周期原子中最小的.