题目内容
7.可逆反应发生下列变化,平衡一定正向移动的是( )| A. | 正反应速率增大 | B. | 反应物浓度减小 | ||
| C. | K值减小 | D. | 正反应速率大于逆反应速率 |
分析 化学反应达到平衡状态,正逆反应速率相同,当正反应速率大于逆反应速率,平衡一定正向移动;
解答 解;A.正反应速率增大平衡不一定发生移动,如加入催化剂正逆反应速率都增大,平衡不变,故A错误;
B.对于反应前后气体体积不变的反应,增大体积,反应物浓度减小,但压强减小平衡不变,故B错误;
C.平衡常数随温度变化,改变压强或浓度平衡可能逆向进行,平衡常数减小,故C错误;
D.可逆反应改变条件当正反应速率大于逆反应速率,平衡一定正向移动,故D正确;
故选D.
点评 本题考查了化学平衡、平衡常数、反应速率影响因素的分析判断,化学平衡移动原理和反应特征的理解应用是解题关键,题目较简单.

练习册系列答案
相关题目
19.下列对如图所示实验装置的判断中正确的是( )
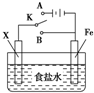

| A. | 若X为锌棒,开关K置于A处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法 | |
| B. | 若 X 为锌棒,开关 K 置于 A 或 B 处均可减缓铁的腐蚀 | |
| C. | 若X为铜棒,开关K置于A处,装置中发生的总反应为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑ | |
| D. | 若X为碳棒,开关K置于B处,向食盐水中滴入酚酞溶液可看到铁棒附近先变红 |
20.下列有关硫酸四氨合铜溶液的叙述正确的是( )
| A. | 该溶液中H+、NH4+、NO3-、Cl-可以大量共存 | |
| B. | Cu(NH3)4SO4中呈正四面体的原子团只有SO42- | |
| C. | 滴加Na2CO3溶液产生CuCO3蓝色沉淀 | |
| D. | 硫酸铜溶液与氨水作用后可缓缓加入乙醇可产生晶体,其产生晶体的主要原理是CuSO4+4NH3═[Cu(NH3)4]SO4 |
17.已知某元素的一种原子可用符号AZX表示,则比其中子数大1的同位素原子的质子数是( )
| A. | Z | B. | A | C. | A+Z+1 | D. | A-Z+1 |
2.某实验小组只领取到下列仪器或用品:烧杯、铁架台、铁圈、三脚架、分液漏斗、酒精灯、漏斗、滤纸、石棉网、量筒、玻璃棒、蒸发皿、圆底烧瓶、火柴.从缺乏仪器的角度看,不能进行的实验操作项目有( )
| A. | 蒸发 | B. | 过滤 | C. | 萃取 | D. | 蒸馏 |
12.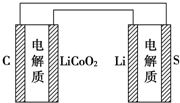 已知电池的比能量是参与电极反应的单位质量的电极材料放出电能的大小.有关下述两种电池说法正确的是( )
已知电池的比能量是参与电极反应的单位质量的电极材料放出电能的大小.有关下述两种电池说法正确的是( )
锂离子电池的总反应为:LixC+Li1-xCoO2$?_{充电}^{放电}$C+LiCoO2
锂硫电池的总反应为:2Li+S$?_{充电}^{放电}$Li2S.
 已知电池的比能量是参与电极反应的单位质量的电极材料放出电能的大小.有关下述两种电池说法正确的是( )
已知电池的比能量是参与电极反应的单位质量的电极材料放出电能的大小.有关下述两种电池说法正确的是( )锂离子电池的总反应为:LixC+Li1-xCoO2$?_{充电}^{放电}$C+LiCoO2
锂硫电池的总反应为:2Li+S$?_{充电}^{放电}$Li2S.
| A. | 锂离子电池放电时,Li+向负极迁移 | |
| B. | 锂硫电池充电时,锂电极发生还原反应 | |
| C. | 理论上两种电池的比能量相同 | |
| D. | 如图表示用锂离子电池给锂硫电池充电 |
19.一定条件下合成乙烯:6H2(g)+2CO2(g)$\stackrel{催化剂}{?}$ CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是( )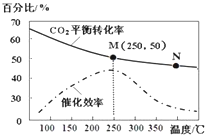

| A. | 生成乙烯的速率:v(M)一定小于v(N) | |
| B. | 化学平衡常数:KN>KM | |
| C. | 当温度高于250℃时,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低 | |
| D. | 若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7% |
16.关于如图所示原电池的说法正确的是( )
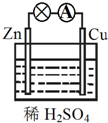

| A. | Zn为正极,Cu为负极 | B. | 该装置将化学能转变为电能 | ||
| C. | 正极反应式为Cu-2e-═Cu2+ | D. | 电子由铜片通过导线流向锌片 |
 (1)CH3OH是一种可燃性的液体.
(1)CH3OH是一种可燃性的液体.