题目内容
实验室有一瓶久置的K2SO3粉末,为确定其是否变质进行的下述实验结论正确的是( )
| A、进行元素分析,测得粉末中K和S两种元素的质量比为39:16,则该粉末没有变质 |
| B、将粉末溶于水,加入氯化钡,有白色沉淀生成,则该粉末变质了 |
| C、将粉末加入盐酸中,产生气泡,则该粉末没有变质 |
| D、将粉末溶于水,滴加过量的盐酸,有气泡产生,再加入氯化钡溶液,有白色沉淀生成,则该粉末部分变质 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:如K2SO3被氧化可生成K2SO4,加入氯化钡都生成沉淀,检验是否变质,应加入过量盐酸除去SO32-,在加入氯化钡进行检验,如有沉淀生成,可证明变质,以此解答.
解答:
解:A.钾和硫的质量比为39:16,则钾原子与硫原子的物质的量之比为
:
=2:1,而硫酸钾与亚硫酸钾中钾原子与硫原子的物质的量之比都为2:1,所以白色粉末可能是亚硫酸钾或硫酸钾或为硫酸钾与亚硫酸钾的混合物,不能证明是否变质,故A错误;
B.若白色粉末是亚硫酸钾或硫酸钾与亚硫酸钾的混合物,溶于水与氯化钡反应也生成白色沉淀,故B错误;
C.白色粉末为硫酸钾与亚硫酸钾的混合物,加入盐酸也产生二氧化硫气体,故C错误;
D.加入盐酸有气泡,说明溶液中含有亚硫酸根,盐酸同时排除亚硫酸根对检验硫酸根的干扰,加入氯化钡有白色沉淀生成,说明溶液中含有硫酸根,证明原粉末是硫酸钾和亚硫酸钾的混合物,可证明部分变质,故D正确.
故选D.
| 39g |
| 39g/mol |
| 16g |
| 32g/mol |
B.若白色粉末是亚硫酸钾或硫酸钾与亚硫酸钾的混合物,溶于水与氯化钡反应也生成白色沉淀,故B错误;
C.白色粉末为硫酸钾与亚硫酸钾的混合物,加入盐酸也产生二氧化硫气体,故C错误;
D.加入盐酸有气泡,说明溶液中含有亚硫酸根,盐酸同时排除亚硫酸根对检验硫酸根的干扰,加入氯化钡有白色沉淀生成,说明溶液中含有硫酸根,证明原粉末是硫酸钾和亚硫酸钾的混合物,可证明部分变质,故D正确.
故选D.
点评:本题考查较为综合,注意亚硫酸根对硫酸根检验的干扰,把握常见离子的检验方法为解答的关键,本题综合考查学生的分析能力、实验能力和评价能力,为高考常见题型,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组稀溶液中,利用组内物质的相互反应,就能将各种物质鉴别出来的是( )
| A、Fe(NO3)3、NaOH、CuSO4、KCl |
| B、KCl、AgNO3、HCl、HNO3 |
| C、CuSO4、NaCl、KNO3、BaCl2 |
| D、BaCl2、Na2SO4、Na2CO3、HCl |
将下列各组物质混合后,溶液中一定有沉淀生成的是( )
| A、Al2(SO4)3溶液与过量氨水 |
| B、NaOH溶液与AlCl3溶液 |
| C、NaAlO2溶液与盐酸 |
| D、少量CO2通入CaCl2溶液 |
聚合硫酸铁(PFS)是一种新型高效的无机高分子净水剂,它的溶液中SO42-与Fe3+物质的量之比不是3:2.为了测定聚合硫酸铁溶液中SO42-与Fe3+物质的量之比需选用的试剂是( )
| A、NaOH |
| B、FeSO4 |
| C、BaCl2 |
| D、NaClO3 |
配制200ml0.1mol/L稀硫酸溶液时,下列实验操作使得所配溶液浓度偏小的是( )
| A、用量筒量取所需的浓硫酸时仰视读数 |
| B、定容后摇匀,发现液面最低点低于刻度线,再补加几滴蒸馏水至刻度线 |
| C、定容时,俯视刻度线 |
| D、用量筒量取浓硫酸倒入烧杯,再用蒸馏水洗量筒2~3次,洗液倒入烧杯中 |
用惰性电极电解下列溶液,一段时间后,加入一定质量的另一种物质(括号中),溶液能与原溶液完全相同的是( )
| A、CuCl2(CuSO4) |
| B、NaOH(H2O) |
| C、AgNO3 (AgNO3) |
| D、CuSO4(Cu2O) |
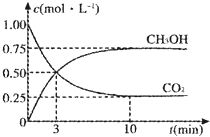 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.