题目内容
化学键使得一百多种元素构成了世界的万事万物,关于化学键的下列叙述中,正确的是( )
| A、离子化合物一定含有共价键,共价化合物中不含离子键 |
| B、共价化合物可能含离子键,离子化合物中只含离子键 |
| C、构成单质分子的粒子一定含有共价键 |
| D、在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用 |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:A.离子化合物可能含共价键,一定含离子键;
B.含离子键的化合物一定为离子化合物;
C.稀有气体中不存在化学键;
D.氧化钠中含离子键.
B.含离子键的化合物一定为离子化合物;
C.稀有气体中不存在化学键;
D.氧化钠中含离子键.
解答:
解:A.离子化合物不一定含有共价键,如NaCl中不含共价键,而共价化合物中一定不含离子键,故A错误;
B.共价化合物一定不含离子键,离子化合物中含离子键,可能含共价键,故B错误;
C.构成单质分子的粒子不一定含有共价键,如稀有气体,故C错误;
D.在氧化钠中,含离子键,则除氧离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用,故D正确;
故选D.
B.共价化合物一定不含离子键,离子化合物中含离子键,可能含共价键,故B错误;
C.构成单质分子的粒子不一定含有共价键,如稀有气体,故C错误;
D.在氧化钠中,含离子键,则除氧离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用,故D正确;
故选D.
点评:本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,注重基础知识的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列元素中,属于第二周期的是( )
| A、氢 | B、氧 | C、钠 | D、氯 |
下列各组比较不正确的是( )
| A、酸性:H4SiO4<H3PO4<H2SO4<HClO4 |
| B、碱性:Be(OH)2<Mg(OH)2<KOH |
| C、氧化性:S<O2<F2 |
| D、还原性:Se2-<S2-<O2- |
下列物质中含有共价键的离子化合物是( )
| A、CaC2 |
| B、MgCl2 |
| C、SiO2 |
| D、C2H4 |
分子式为C5H12O且催化氧化后能发生银镜反应的有机化合物有(不考虑立体异构)( )
| A、4种 | B、5种 | C、6种 | D、7种 |
下列说法正确的是( )
| A、第ⅠA族金属单质的密度、熔沸点均随着核电荷数的增大而递增 |
| B、金属锂在氧气中燃烧生成Li2 O2 |
| C、金属的还原性:Li>Na>K>Rb |
| D、氢化物的稳定性:HF>HCl>HBr>HI |
在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是( )
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
| A、该变化的基本反应类型是分解反应 |
| B、反应后物质M的质量为l3g |
| C、反应中N、P的质量比为5:4 |
| D、物质Q可能是该反应的催化剂 |
下列化学用语表达不正确的是( )
A、二氧化碳的电子式: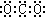 |
| B、水分子的结构式:H-O-H |
C、乙烯的比例模型: |
| D、碳酸氢钠溶于水的电离方程式:NaHCO3=Na++HCO3- |
实验室用铅蓄电池作电源电解饱和食盐水制取氯气.已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42--2e-=PbSO4 正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
今若制取0.25mol Cl2,这时电池内消耗的H2SO4的物质的量至少是( )
负极:Pb+SO42--2e-=PbSO4 正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
今若制取0.25mol Cl2,这时电池内消耗的H2SO4的物质的量至少是( )
| A、0.25 mol |
| B、0.35 mol |
| C、0.50mol |
| D、0.75mol |