题目内容
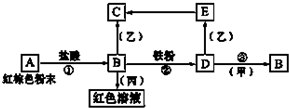 下列物质之间有如图反应关系:已知由E转化成C的现象是灰白色沉淀迅速变为灰绿色,最后变为红褐色.回答:
下列物质之间有如图反应关系:已知由E转化成C的现象是灰白色沉淀迅速变为灰绿色,最后变为红褐色.回答:(1)写出下列物质的化学式:
A
(2)写出E→C反应的化学方程式:
(3)写出反应①的离子方程式:
(4)写出反应②的离子方程式:
(5)写出反应③的离子方程式:
考点:无机物的推断
专题:推断题
分析:E转化成C的现象是灰白色沉淀迅速变为灰绿色,最后变为红褐色,则E是Fe(OH)2、C是Fe(OH)3,
A是红棕色粉末,能和盐酸反应生成B,则A是Fe2O3、B是FeCl3,B和丙反应生成红色溶液,则丙是KSCN,B和Fe反应生成D,则D是FeCl2,D和乙反应生成Fe(OH)2,则乙是NaOH溶液,D和甲反应生成FeCl3,则甲是Cl2,再结合题目分析解答.
A是红棕色粉末,能和盐酸反应生成B,则A是Fe2O3、B是FeCl3,B和丙反应生成红色溶液,则丙是KSCN,B和Fe反应生成D,则D是FeCl2,D和乙反应生成Fe(OH)2,则乙是NaOH溶液,D和甲反应生成FeCl3,则甲是Cl2,再结合题目分析解答.
解答:
解:E转化成C的现象是灰白色沉淀迅速变为灰绿色,最后变为红褐色,则E是Fe(OH)2、C是Fe(OH)3,
A是红棕色粉末,能和盐酸反应生成B,则A是Fe2O3、B是FeCl3,B和丙反应生成红色溶液,则丙是KSCN,B和Fe反应生成D,则D是FeCl2,D和乙反应生成Fe(OH)2,则乙是NaOH溶液,D和甲反应生成FeCl3,则甲是Cl2,
(1)通过以上分析知,A、B、D、甲、乙、丙分别是Fe2O3、FeCl3、FeCl2、Cl2、NaOH、KSCN,
故答案为:Fe2O3;FeCl3;FeCl2;Cl2;NaOH;KSCN;
(2)E→C反应的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)反应①的离子方程式:Fe2O3+6H+=2Fe3++3H2O,故答案为:Fe2O3+6H+=2Fe3++3H2O;
(4)反应②的离子方程式:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(5)反应③的离子方程式:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-.
A是红棕色粉末,能和盐酸反应生成B,则A是Fe2O3、B是FeCl3,B和丙反应生成红色溶液,则丙是KSCN,B和Fe反应生成D,则D是FeCl2,D和乙反应生成Fe(OH)2,则乙是NaOH溶液,D和甲反应生成FeCl3,则甲是Cl2,
(1)通过以上分析知,A、B、D、甲、乙、丙分别是Fe2O3、FeCl3、FeCl2、Cl2、NaOH、KSCN,
故答案为:Fe2O3;FeCl3;FeCl2;Cl2;NaOH;KSCN;
(2)E→C反应的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)反应①的离子方程式:Fe2O3+6H+=2Fe3++3H2O,故答案为:Fe2O3+6H+=2Fe3++3H2O;
(4)反应②的离子方程式:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(5)反应③的离子方程式:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-.
点评:本题以Fe及其化合物为载体考查无机物推断,以E生成C颜色变化为题眼采用正逆结合的方法进行推断,知道铁离子、亚铁离子检验方法及现象,知道离子方程式书写规则即物质性质即可解答,题目难度中等.

练习册系列答案
相关题目
化学与生活、社会密切相关.下列叙述不正确的是( )
| A、生物柴油具有良好的燃料性能,且安全、环保、可再生,它的成分是高级脂肪酸甲酯或乙酯 |
| B、PM2.5的颗粒物,分散在空气中可形成胶体 |
| C、制造生活中的水杯、奶瓶、食物保鲜膜等,使用聚乙烯材料比聚氯乙烯更有利于健康 |
| D、甘油与汽油都不属于化学意义上的油 |