题目内容
日本发生的9.0级大地震造成了福岛核电站发生了严重的核泄漏事故,我国除广西外均检测到了放射性物质碘-131(
I),其中子数与核外电子数之差为( )
131 53 |
| A、26 | B、25 | C、78 | D、32 |
考点:质子数、中子数、核外电子数及其相互联系
专题:原子组成与结构专题
分析:原子中,中子数=质量数-质子数,核外电子数=核电荷数,据此分析解答.
解答:
解:
I的原子中质子数为53,质量数为131,中子数=质量数-质子数=131-53=78,由题意知核外电子数等于核电荷数为53,该同位素原子核内的中子数与核外电子数之差为:78-53=25.
故选B.
131 53 |
故选B.
点评:本题考查质子数、中子数、核外电子数及其相互联系,题目难度不大,明确在原子中:质子数=电子数=核电荷数;相对原子质量=质子数+中子数是解题的关键.

练习册系列答案
相关题目
德国哈伯发明以低成本制造大量氨的方法,流程图中为提高原料转化率而采取措施是( )
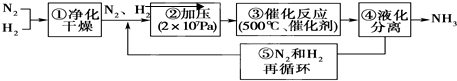

| A、①②③ | B、②④⑤ |
| C、①③⑤ | D、②③④ |
设阿伏伽德罗常数的数值为NA,下列说法正确的是( )
| A、5.6g铁与足量的Cl2反应失去电子数为0.2NA个 |
| B、标况下22.4L O2和O3组成的混合物中总原子数为2NA个 |
| C、常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
| D、1 L l mol?L-1的氯化铁溶液中铁离子Fe3+的数目为NA |
下列递变规律正确的是( )
| A、HClO4、H2SO4、H3PO4的酸性依次增强 |
| B、P、S、Cl最高正价依次降低 |
| C、钠、镁、铝的还原性依次减弱 |
| D、HCl、HBr、HI的稳定性依次增强 |
在室温条件下,保存下列药品的正确方法是( )
| A、用密闭的塑料瓶保存氢氟酸 |
| B、用玻璃塞的试剂瓶保存NaOH溶液 |
| C、用无色试剂瓶保存氯水 |
| D、碘存放在用蜡封口的瓶中 |
某气态烃在一个密闭容器中和过量的氧气混合完全燃烧,反应后测得容器内压强不变(温度为120℃),此气态烃为( )
| A、CH4 |
| B、C2H4 |
| C、C3H6 |
| D、C3H8 |
酒精燃烧的化学方程式为:C2H6O+3O2═2CO2+3H2O,完全燃烧一定量的无水酒精,放出的热量为Q,当完全吸收生成的CO2,消耗8mol/L的NaOH溶液50ml时恰好生成正盐.则燃烧1mol无水酒精所放出的热量为( )
| A、0.2Q | B、0.1Q |
| C、5Q | D、10Q |
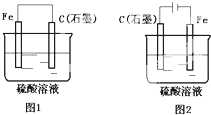 如图是化学能与电能相互转换的两套装置.对此两套装置的分析正确的是( )
如图是化学能与电能相互转换的两套装置.对此两套装置的分析正确的是( )| A、两装置中,铁电极上均有气体产生 |
| B、两装置中,石墨电极上均有气体产生 |
| C、石墨电极上发生的电极反应均为:2H++2e-=H2↑ |
| D、随着反应的进行,两装置中电解质溶液的酸性均减弱 |
设NA为阿伏加德罗常数的值.下列说法不正确的是( )
| A、常温常压下,13.8g NO2气体溶于足量水,转移电子数为0.2NA |
| B、标准状况下,22.41.CH3CI含有的原子数为5NA |
| C、0.5mo1O2与11.2LO2所含的分子数一定相等 |
| D、常温常压下,14g乙烯与丙烯的混合气体,含碳原子总数为NA |