题目内容
2.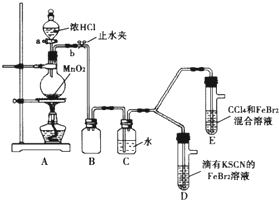 某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验:
某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验:(1)①连接仪器:把玻璃导管插入橡胶塞的操作是:将玻璃导管插入带孔橡皮塞时,应先将要插入塞子的玻璃导管的一端用水润湿(水起润滑作用),然后对准橡胶塞上的孔稍稍用力转动,将其插入.
②检查装置A的气密性的操作是关闭止水夹b,打开活塞a;然后向分液漏斗中注水,若水不能顺利流下,则气密性良好.
③装置A中发生反应的离子方程式为MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O.
④整套实验装置存在一处明显不足,请指出:缺少尾气处理装置.
(2)用改正后的装置进行实验.实验过程如下:
①实验操作:打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯.
②实验现象:装置D中溶液变红,装置E中水层溶液变黄,振荡后CCl4层无明显变化,则装置D中发生反应的离子方程式是2Fe2++Cl2=2Fe3++2Cl-.
③结论:Cl2、Br2、Fe3+的氧化性由强到弱的顺序为Cl2>Br2>Fe3+.
分析 (1)①将玻璃导管插入带孔橡皮塞的方法注意左软右硬,用水湿润后连接;
②装置A制备氯气,装置连接后应检验装置的气密性,可以利用分液漏斗中的液体是否流下分析判断装置气密性;
③A中发生的反应是二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水;
④氯气有毒不能直接排空,应该有尾气处理装置处理尾气;
(2)氯气能氧化亚铁离子生成铁离子,铁离子和KSCN反应生成络合物硫氰化铁而使溶液呈血红色;氯气和溴离子发生置换反应生成溴单质,溴易溶于四氯化碳而使溶液呈棕色,自发进行的同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
解答 解:(1)①连接玻璃导管和胶皮管的正确操作是:将玻璃导管插入带孔橡皮塞时,应先将要插入塞子的玻璃导管的一端用水润湿(水起润滑作用),然后稍用力转动使之插入橡皮塞内,
故答案为:将玻璃导管插入带孔橡皮塞时,应先将要插入塞子的玻璃导管的一端用水润湿(水起润滑作用);
②装置A制备氯气,装置连接后应检验装置的气密性,方法是关闭止水夹b,打开活塞a,向分液漏斗中注水,若水不能顺利流下,则气密性良好,
故答案为:关闭止水夹b,打开活塞a;
③A中发生的反应是二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,反应的离子方程式为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O;
④氯气有毒不能直接排空,应该有尾气处理装置处理尾气,否则易产生污染,故答案为:缺少尾气处理装置;
(2)实验现象:装置D中溶液变红,装置E中水层溶液变黄,振荡后CCl4层无明显变化说明氯气和溴离子不反应,D中反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,
D装置中:溶液变红,说明有铁离子生成,据此得出氯气的氧化性大于铁离子;
E装置中:水层溶液变黄,振荡后CCl4层无明显变化,说明氯气和溴离子不反应,
根据D和E装置知,溴的氧化性大于铁离子,则氧化性强弱顺序是 Cl2>Br2>Fe3+,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;Cl2>Br2>Fe3+;
点评 本题考查了性质实验方案设计,明确反应原理是解本题关键,结合资料分析解答,会根据离子反应方程式判断氧化性强弱,会根据实验现象确定发生的反应,难度中等.

| A. | pH=5的 H2S溶液中,c(H+)=c(HS-)=1×10-5mol/L | |
| B. | 稀释氨水溶液10倍后,其c(OH-)为原來的$\frac{1}{10}$ | |
| C. | pH之和为14的 H2C2O4与NaOH 溶液混合:c(Na+)+c(H+)=c(OH-)+C(HC2O4-) | |
| D. | 将等物质的费的Na2CO3和NaHCO3混合溶于水中:$\frac{c(C{O}_{{3}^{2-}})}{c(HC{O}_{{3}^{-}})}$<1 |
| A. | 金属钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | NaHCO3的水解反应:HCO3-+H2O?CO32-+H3O+ | |
| C. | 铁和稀HNO3反应后溶液pH=1:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | 向Mg(HCO3)2溶液中加入过量NaOH溶液:Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O |

| A. | 溶液的pH:①>②>③ | |
| B. | 整个过程中Fe2(SO4)3溶液可以循环利用 | |
| C. | 溶液②转化为溶液③发生反应的离子方程式为4H++4Fe2++O2=4Fe3++2H2O | |
| D. | 向②溶液中滴加KSCN溶液,溶液可能变为血红色 |
| A. | 6:3:2 | B. | 1:2:3 | C. | 3:2:1 | D. | 1:1:1 |

| A. | 同温同压下,只要物质比例适当,从正、逆方向都可以建立同一平衡状态 | |
| B. | 图甲表示的反应为H2(g)+I2(g)?2HI(g) | |
| C. | 图甲中H2的转化率+图乙中HI的转化率=100% | |
| D. | 相同条件下,分别从正、逆方向建立等同的平衡状态,所需时间相同 |
| A. | 常温下能够使pH试纸显红色的溶液 | B. | 常温下能够使甲基橙显黄色的溶液 | ||
| C. | [OH-]>[H+]的溶液 | D. | 加入MgCl2生成白色沉淀的溶液 |
| A. | NaCl溶液 | B. | NaOH溶液 | C. | CH3COOK溶液 | D. | NH4Cl溶液 |
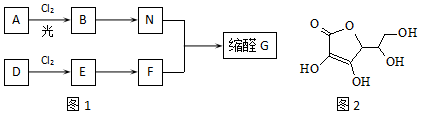
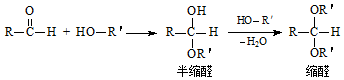
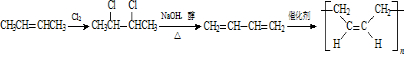
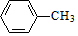 ,E的名称是1,2-二氯乙烷.
,E的名称是1,2-二氯乙烷.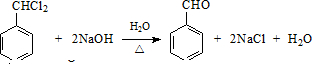 .
.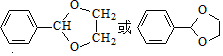 .G有多种同分异构体,写出其中能同时满足以下条件的所有同分异构体的结构简式:
.G有多种同分异构体,写出其中能同时满足以下条件的所有同分异构体的结构简式: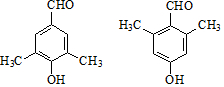 .
. .
.