题目内容
10.下列说法正确的是( )| A. | 常温下用二氧化锰和浓盐酸反应制取Cl2 | |
| B. | 用饱和氯化钠溶液可以洗涤除去氯化钠固体表面少量氯化钾杂质 | |
| C. | 向某溶液中加入盐酸酸化的BaCl2溶液,产生白色沉淀,可知该溶液中一定含有SO42- | |
| D. | 向浓度均为0.01mol/L的K2SO4和KI混合溶液中滴加Pb(NO3)2溶液,先生成PbI2黄色沉淀 |
分析 A.二氧化锰与浓盐酸加热发生氧化还原反应生成氯气;
B.洗涤氯化钠固体,应尽量避免固体的溶解,且不能引入杂质;
C.白色沉淀为硫酸钡或AgCl;
D.PbSO4、PbI2的溶度积常数分别为1.8×10-8、7.0×10-9.
解答 解:A.二氧化锰与浓盐酸加热发生氧化还原反应生成氯气,常温下不反应,故A错误;
B.氯化钠饱和溶液中存在NaCl(s)?Na+(aq)+Cl-(aq),可用饱和食盐水洗涤,以避免引入新杂质,且减少氯化钠的溶解,可洗涤,故B正确;
C.白色沉淀为硫酸钡或AgCl,溶液中可能含有SO42-或银离子,但二者不能同时存在,故C错误;
D.出现沉淀时的铅离子浓度依次为$\frac{1.8×1{0}^{-8}}{0.01}$=1.8×10-6、$\frac{7.0×1{0}^{-9}}{0.0{1}^{2}}$=7.0×10-5,则先生成PbSO4沉淀,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握气体的制备实验、溶解平衡、离子检验、Ksp的应用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
1.下列说法中,正确的是( )
| A. | 液氯和氯水都含有氯离子 | |
| B. | 氯气和液氯都能使干燥的有色布条褪色 | |
| C. | 盐酸和氯水都含有氯离子 | |
| D. | 盐酸和氯水都能使湿润的有色布条褪色 |
18.下列仪器名称为“烧杯”的是( )
| A. | 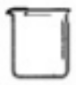 | B. |  | C. | 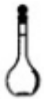 | D. | 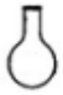 |
5.下列说法正确的是( )
| A. | lmol葡萄糖能水解生成2molCH3CH2OH和2molCO2 | |
| B. | 苯的结构简式为 ,能使酸性高锰酸钾溶液褪色 ,能使酸性高锰酸钾溶液褪色 | |
| C. | 相同物质的量的乙烯与乙醇分别在足量的O2中完全燃烧,消耗O2的物质的量相同 | |
| D. | 乙烯和植物油都能使溴水褪色,其褪色原理不同 |
15.诺氟沙星别名氟哌酸,是治疗肠炎痢疾的常用药.其结构简式如图,下列说法正确的是( )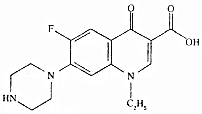

| A. | 该化合物属于苯的同系物 | |
| B. | 分子式为Cl6 H16FN3O3 | |
| C. | 1mol该化合物中含有6NA个双键 | |
| D. | 该化合物能与酸性高锰酸钾、溴水、碳酸氢钠溶液反应 |
2.下列溶液中微粒的物质的量浓度关系一定正确的是( )
| A. | 某温度下,pH=7的NH4Cl与NH3•H2O的混合溶液:c(NH4+)=c(Cl-)>c(H+)=c(OH-) | |
| B. | 0.1 mol/L Na2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | 25℃时,pH=2的HCOOH与pH=12的NaOH等体积混合:c(HCOO-)<c(Na+) | |
| D. | 0.1 mol/L Na2CO3溶液与0.1 mol/L NaHCO3溶液等体积混合:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+) |
6.醋酸溶液中存在电离平衡CH3COOH?H++CH3COO-,下列叙述正确的是( )
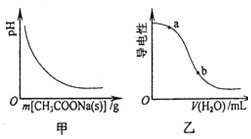

| A. | 图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 | |
| B. | 图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b | |
| C. | 醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) | |
| D. | 0.10 mol•L-1的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 |
7.在某温度下,将2molA和3molB充入一密闭容器中,发生反应:aA(g)+B(g)?C(g)+D(g),5min后达到平衡,测得K=1.若在温度不变的情况下将容器的体积扩大为原来的1倍,测得A的转化率不发生变化,下列说法正确的是( )
| A. | 改变条件前后,B的转化率均为40% | |
| B. | 改变条件前后,C的反应速率保持不变 | |
| C. | 若保持温度和体积不变,在容器中再充入1molA和1molB,B的转化率不变 | |
| D. | 若保持温度和体积不变,在容器中再充入0.5molB、1molC和1molD,B的转化率增大 |