题目内容
在标准状况下,取甲、乙、丙各100mL相同浓度的盐酸,分别加入组成相同的镁铝合金粉末,得到的气体体积(标准状况)与合金的质量有关数据如下表;
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 2.55 | 3.85 | 4.59 |
| 气体体积/L | 2.80 | 3.36 | 3.36 |
- A.甲组中盐酸过量,丙组中金属过量
- B.盐酸的物质的量浓度为1mol/L
- C.合金中镁,铝的物质的量之比是1:1
- D.向甲容器中继续加入350mL1.00mol?L-1NaOH溶液时,生成沉淀0.1mol
BD
分析:甲中加入2.55g合金时生成气体的体积为2.80L,继续加入合金,最多生成3.36L气体,说明甲中盐酸过量,且生成气体最多为3.36L,根据反应的相关方程式计算.
解答:A.甲中加入2.55g合金时生成气体的体积为2.80L,继续加入合金,最多生成3.36L气体,说明甲中盐酸过量,金属不足,分别加入金属3.85g和4.59g时,生成气体的体积相等,则说明丙组中金属过量,故A正确;
B.不管加多少镁铝合金,最多只能生成3.36L的氢气,说明盐酸最多只能产生3.36L的氢气.所以就3.36L来计算盐酸的物质的量. 气体的物质的量为: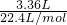 =0.15mol,
=0.15mol,
根据方程式,可计算出HCl的物质的量为0.15mol×2=0.3mol,盐酸的物质的量浓度为: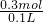 =3mol/L,故B错误;
=3mol/L,故B错误;
C.由于甲组中,盐酸是过量的,所以用甲组来计算,设Mg的物质的量为x,Al的物质的量为y,
生成气体的物质的量为: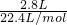 =0.125mol,
=0.125mol,
依题意得:24x+27y=2.55g;x+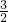 y=0.125mol,
y=0.125mol,
解方程组得:x=0.05;y=0.05,
所以物质的量之比为1:1,
故C正确;
D.当甲中Mg2+、Al3+全部生成沉淀时,溶液的溶质为NaCl,已知n(Cl-)=0.15mol×2=0.3mol,则需1.00mol?L-1NaOH溶液
300ml,此时加入350mL1.00mol?L-1NaOH溶液,则有Al(OH)3+OH-=AlO2-+2H2O,所以沉淀的物质的量小于0.1mol,故D错误;
故选BD.
点评:本题考查混合物的计算,题目难度较大,注意根据表中数据判断合金与盐酸反应的过量问题为解答本题的关键.
分析:甲中加入2.55g合金时生成气体的体积为2.80L,继续加入合金,最多生成3.36L气体,说明甲中盐酸过量,且生成气体最多为3.36L,根据反应的相关方程式计算.
解答:A.甲中加入2.55g合金时生成气体的体积为2.80L,继续加入合金,最多生成3.36L气体,说明甲中盐酸过量,金属不足,分别加入金属3.85g和4.59g时,生成气体的体积相等,则说明丙组中金属过量,故A正确;
B.不管加多少镁铝合金,最多只能生成3.36L的氢气,说明盐酸最多只能产生3.36L的氢气.所以就3.36L来计算盐酸的物质的量. 气体的物质的量为:
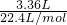 =0.15mol,
=0.15mol,根据方程式,可计算出HCl的物质的量为0.15mol×2=0.3mol,盐酸的物质的量浓度为:
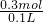 =3mol/L,故B错误;
=3mol/L,故B错误;C.由于甲组中,盐酸是过量的,所以用甲组来计算,设Mg的物质的量为x,Al的物质的量为y,
生成气体的物质的量为:
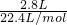 =0.125mol,
=0.125mol,依题意得:24x+27y=2.55g;x+
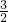 y=0.125mol,
y=0.125mol,解方程组得:x=0.05;y=0.05,
所以物质的量之比为1:1,
故C正确;
D.当甲中Mg2+、Al3+全部生成沉淀时,溶液的溶质为NaCl,已知n(Cl-)=0.15mol×2=0.3mol,则需1.00mol?L-1NaOH溶液
300ml,此时加入350mL1.00mol?L-1NaOH溶液,则有Al(OH)3+OH-=AlO2-+2H2O,所以沉淀的物质的量小于0.1mol,故D错误;
故选BD.
点评:本题考查混合物的计算,题目难度较大,注意根据表中数据判断合金与盐酸反应的过量问题为解答本题的关键.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
在标准状况下,取甲、乙、丙各100mL相同浓度的盐酸,分别加入组成相同的镁铝合金粉末,得到的气体体积(标准状况)与合金的质量有关数据如下表;
|
在标准状况下,取甲、乙、丙各30.0 mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉末,得下表有关数据(假设反应前后溶液体积不发生变化):
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 255 | 385 | 459 |
气体体积/mL | 280 | 336 | 336 |
试完成下列问题:
(1)甲组实验中,盐酸(选填“过量”“适量”或“不足量”,下同)__________;乙组实验中盐酸____________。
(2)盐酸的物质的量浓度是多少?
(3)合金中镁、铝的物质的量之比为多少?
(4)丙实验之后,向容器中加入一定量的1.00 mol·L-1NaOH溶液,能使合金中的铝粉恰好完全溶解,再过滤出不溶性固体,求所得滤液中各溶质的物质的量浓度。
在标准状况下,取甲、乙、丙各100mL相同浓度的盐酸,分别加入组成相同的镁铝合金粉末,得到的气体体积(标准状况)与合金的质量有关数据如下表;
则下列说法错误的是( )
A.甲组中盐酸过量,丙组中金属过量
B.盐酸的物质的量浓度为1mol/L
C.合金中镁,铝的物质的量之比是1:1
D.向甲容器中继续加入350mL1.00mol?L-1NaOH溶液时,生成沉淀0.1mol
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 2.55 | 3.85 | 4.59 |
| 气体体积/L | 2.80 | 3.36 | 3.36 |
A.甲组中盐酸过量,丙组中金属过量
B.盐酸的物质的量浓度为1mol/L
C.合金中镁,铝的物质的量之比是1:1
D.向甲容器中继续加入350mL1.00mol?L-1NaOH溶液时,生成沉淀0.1mol
