题目内容
 某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出).
某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出).实验选用铜片、98.3%的H2SO4、品红溶液、澄清石灰水、CCl4、NaOH溶液等药品,铜片一端没入浓H2SO4中,另一端露置在液面上方.
回答下列问题.
(1)Cu与浓H2SO4的反应的化学方程式为
(2)D、E两容器中CCl4的作用是
(3)加热过程中,观察到A容器中出现大量白色烟雾,随着反应的进行,A容器下有白色沉淀生成,你认为该沉淀物是
(4)对A容器中的浓H2SO4和铜片进行加热,很快发现C容器中品红溶液褪色,但始终未见D试管中澄清石灰水出现浑浊或沉淀.你的猜想是
(5)实验结束后,为了减少环境污染,排除各装置中的SO2,可采取的操作是
考点:浓硫酸的性质实验
专题:
分析:(1)浓硫酸和Cu共热反应生成硫酸铜、二氧化硫、水,依此写出化学方程式;
(2)二氧化硫和强碱的反应十分剧烈,要注意防止倒吸现象的发生;
(3)铜和浓硫酸反应生成硫酸铜,加热的情况下,由于A容器中出现大量白色烟雾,导致溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜;
(4)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,说明产生SO2气体的速率快,但始终未见D试管中澄清石灰水出现浑浊或沉淀,这是由于SO2溶解度较大,立即生成了Ca(HSO3)2溶液的缘故.因此验证猜想的方法是取样后,向其中加入氢氧化钠溶液,观察是否有沉淀生成(或者加热、加盐酸检验SO2气体等方法);
(5)二氧化硫为酸性气体,可用浓氢氧化钠溶液吸收,减小对环境的污染.
(2)二氧化硫和强碱的反应十分剧烈,要注意防止倒吸现象的发生;
(3)铜和浓硫酸反应生成硫酸铜,加热的情况下,由于A容器中出现大量白色烟雾,导致溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜;
(4)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,说明产生SO2气体的速率快,但始终未见D试管中澄清石灰水出现浑浊或沉淀,这是由于SO2溶解度较大,立即生成了Ca(HSO3)2溶液的缘故.因此验证猜想的方法是取样后,向其中加入氢氧化钠溶液,观察是否有沉淀生成(或者加热、加盐酸检验SO2气体等方法);
(5)二氧化硫为酸性气体,可用浓氢氧化钠溶液吸收,减小对环境的污染.
解答:
解:(1)浓硫酸和Cu共热反应生成硫酸铜、二氧化硫、水,化学方程式为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(2)二氧化硫和强碱的反应十分剧烈,可以采用四氯化碳的作用来达到防止倒吸现象的发生的目的,
故答案为:防止倒吸;
(3)铜和浓硫酸反应生成硫酸铜,加热的情况下,由于A容器中出现大量白色烟雾,导致溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜,
故答案为:CuSO4;铜和浓硫酸反应生成硫酸铜,加热的情况下,由于A容器中出现大量白色烟雾,导致溶剂减少,且浓硫酸具有吸水性;
(4)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,说明产生SO2气体的速率快,但始终未见D试管中澄清石灰水出现浑浊或沉淀,这是由于SO2溶解度较大,立即生成了Ca(HSO3)2溶液的缘故.因此验证猜想的方法是取样后,向其中加入氢氧化钠溶液,观察是否有沉淀生成(或者加热、加盐酸检验SO2气体等方法),
故答案为:SO2溶解度较大,澄清石灰水中Ca(OH)2含量低,生成了Ca(HSO3)2溶液;取样后,向其中加入氢氧化钠溶液,观察是否有沉淀生成(或者加盐酸检验SO2气体等方法);
(5)打开三颈烧瓶的弹簧夹,充入空气把二氧化硫赶到盛有浓氢氧化钠溶液的烧杯中吸收,减小对环境的污染,
故答案为:打开三颈烧瓶的弹簧夹,充入空气把二氧化硫赶到盛有浓氢氧化钠溶液的烧杯中吸收.
| ||
故答案为:Cu+2H2SO4(浓)
| ||
(2)二氧化硫和强碱的反应十分剧烈,可以采用四氯化碳的作用来达到防止倒吸现象的发生的目的,
故答案为:防止倒吸;
(3)铜和浓硫酸反应生成硫酸铜,加热的情况下,由于A容器中出现大量白色烟雾,导致溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜,
故答案为:CuSO4;铜和浓硫酸反应生成硫酸铜,加热的情况下,由于A容器中出现大量白色烟雾,导致溶剂减少,且浓硫酸具有吸水性;
(4)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,说明产生SO2气体的速率快,但始终未见D试管中澄清石灰水出现浑浊或沉淀,这是由于SO2溶解度较大,立即生成了Ca(HSO3)2溶液的缘故.因此验证猜想的方法是取样后,向其中加入氢氧化钠溶液,观察是否有沉淀生成(或者加热、加盐酸检验SO2气体等方法),
故答案为:SO2溶解度较大,澄清石灰水中Ca(OH)2含量低,生成了Ca(HSO3)2溶液;取样后,向其中加入氢氧化钠溶液,观察是否有沉淀生成(或者加盐酸检验SO2气体等方法);
(5)打开三颈烧瓶的弹簧夹,充入空气把二氧化硫赶到盛有浓氢氧化钠溶液的烧杯中吸收,减小对环境的污染,
故答案为:打开三颈烧瓶的弹簧夹,充入空气把二氧化硫赶到盛有浓氢氧化钠溶液的烧杯中吸收.
点评:本题考查了浓硫酸的性质,题目难度中等,注意掌握浓硫酸具有的化学性质,明确性质实验方案设计的方法,明确题中资料信息是解题根据,试题培养了学生的分析、理解能力.

练习册系列答案
相关题目
下列说法中,正确的是( )
| A、两种难溶盐电解质,其中Ksp小的溶解度一定小 |
| B、溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定先沉淀 |
| C、Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
| D、凡是能自发进行的化学反应,一定是△H<0、△S>0 |
用如图所示装置进行下列实验,能达到实验目的是( )
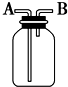

| A、瓶中盛有适量浓H2SO4,从A口进气来干燥NH3 |
| B、从B口进气,用排空气法收集CO2 |
| C、瓶中盛满水,从B口进气,用排水法收集NO2 |
| D、瓶中装满水,A口连接导管并伸入量筒中,从B口进气,用排水法测量生成H2的体积 |
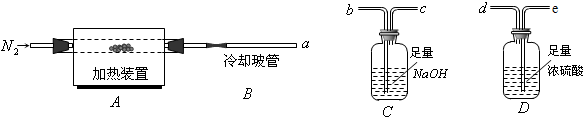

 如图是实验室制取某些气体的装置.
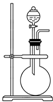
如图是实验室制取某些气体的装置.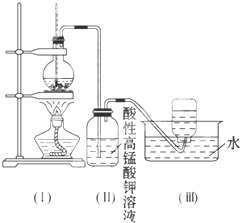 如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯:CH3CH2OH
如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯:CH3CH2OH