题目内容
下列各组物质中,所含分子数相同的是(气体均在标准状况下)
- A.10g H2和10g O2
- B.9g H2O和71g Cl2
- C.5.6L N2和11g CO2
- D.224mL H2和0.1mol N2
C
分析:根据一定条件下物质的物质的量相同,则所含分子数相同,则利用n= ,n=
,n= 来计算解答即可.
来计算解答即可.
解答:A、H2的物质的量为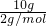 =5mol,O2的物质的量为
=5mol,O2的物质的量为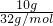 ≈0.3mol,则二者的物质的量不同,即所含分子数不同,故A错误;
≈0.3mol,则二者的物质的量不同,即所含分子数不同,故A错误;
B、H2O的物质的量为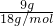 =0.5mol,Cl2的物质的量为
=0.5mol,Cl2的物质的量为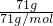 =1mol,则二者的物质的量不同,即所含分子数不同,故B错误;
=1mol,则二者的物质的量不同,即所含分子数不同,故B错误;
C、在标准状况下,Vm=22.4L/mol,则N2的物质的量为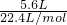 =0.25mol,CO2的物质的量为
=0.25mol,CO2的物质的量为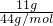 =0.25mol,即物质的量相同、分子数相同,故C正确;
=0.25mol,即物质的量相同、分子数相同,故C正确;
D、在标准状况下,Vm=22.4L/mol,224mL=0.224L,则H2的物质的量为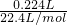 =0.01mol,而N2的物质的量为0.1mol,则二者的物质的量不同,即所含分子数不同,故D错误;
=0.01mol,而N2的物质的量为0.1mol,则二者的物质的量不同,即所含分子数不同,故D错误;
故选C.
点评:本题利用物质的量的计算来分析分子数的关系,明确物质的量相同则分子数相同是解答的关键,学生熟悉常见物质的摩尔质量及标况下气体摩尔体积即可解答.
分析:根据一定条件下物质的物质的量相同,则所含分子数相同,则利用n=
 ,n=
,n= 来计算解答即可.
来计算解答即可.解答:A、H2的物质的量为
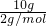 =5mol,O2的物质的量为
=5mol,O2的物质的量为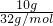 ≈0.3mol,则二者的物质的量不同,即所含分子数不同,故A错误;
≈0.3mol,则二者的物质的量不同,即所含分子数不同,故A错误;B、H2O的物质的量为
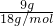 =0.5mol,Cl2的物质的量为
=0.5mol,Cl2的物质的量为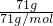 =1mol,则二者的物质的量不同,即所含分子数不同,故B错误;
=1mol,则二者的物质的量不同,即所含分子数不同,故B错误;C、在标准状况下,Vm=22.4L/mol,则N2的物质的量为
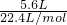 =0.25mol,CO2的物质的量为
=0.25mol,CO2的物质的量为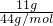 =0.25mol,即物质的量相同、分子数相同,故C正确;
=0.25mol,即物质的量相同、分子数相同,故C正确;D、在标准状况下,Vm=22.4L/mol,224mL=0.224L,则H2的物质的量为
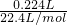 =0.01mol,而N2的物质的量为0.1mol,则二者的物质的量不同,即所含分子数不同,故D错误;
=0.01mol,而N2的物质的量为0.1mol,则二者的物质的量不同,即所含分子数不同,故D错误;故选C.
点评:本题利用物质的量的计算来分析分子数的关系,明确物质的量相同则分子数相同是解答的关键,学生熟悉常见物质的摩尔质量及标况下气体摩尔体积即可解答.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
下列各组物质中,所含分子数相同的是( )
| A、10g H2和10g O2 | B、5.6L N2(标准状况)和11g CO2 | C、11.2L(标准状况)H2O和0.5mol Br2 | D、224mL H2(标准状况)和0.1mol N2 |