题目内容
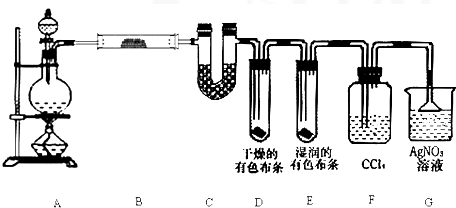
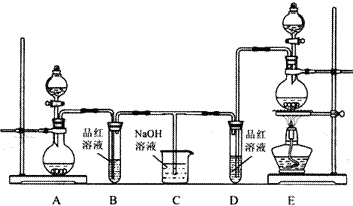
 如下图所示的实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中正确的是( )
如下图所示的实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中正确的是( )分析:(2)能自发的进行氧化还原反应,所以为原电池,则(1)为电解池,锌易失电子作负极,铜作正极,连接锌的碳棒作阴极,连接铜的碳棒作阳极,负极上锌失电子发生氧化反应,正极上氢离子得电子发生还原反应,阳极上氢氧根离子放电生成氧气,阴极上铜离子放电生成铜.
解答:解:(2)能自发的进行氧化还原反应,所以为原电池,则(1)为电解池,锌易失电子作负极,铜作正极,连接锌的碳棒作阴极,连接铜的碳棒作阳极,
A.(1)中产生氧气,(2)中产生氢气,当转移0.02mol电子时生成氧气的体积=
×22.4L/mol=0.112L,生成氢气体积=
×22.4L/mol=0.224L,所以生成气体体积:①<②,故A错误;
B.铜电极上放出氢气体积=
×22.4L/mol=0.224L=224mL,故B正确;
C.(1)中阳极上氢氧根离子放电导致溶液中氢离子浓度增大,溶液的pH减小,(2)中氢离子得电子生成氢气导致氢离子浓度降低,溶液的pH增大,故C错误;
D.(1)中阳极上氢氧根离子放电生成氧气,电极反应式为:4OH--4e-→2H2O+O2↑,②中负极锌失电子生成锌离子,电极反应式为:Zn-2e-→Zn2+,故D错误;
故选B.
A.(1)中产生氧气,(2)中产生氢气,当转移0.02mol电子时生成氧气的体积=
| 0.02mol |
| 4 |
| 0.02mol |
| 2 |
B.铜电极上放出氢气体积=
| 0.02mol |
| 2 |
C.(1)中阳极上氢氧根离子放电导致溶液中氢离子浓度增大,溶液的pH减小,(2)中氢离子得电子生成氢气导致氢离子浓度降低,溶液的pH增大,故C错误;
D.(1)中阳极上氢氧根离子放电生成氧气,电极反应式为:4OH--4e-→2H2O+O2↑,②中负极锌失电子生成锌离子,电极反应式为:Zn-2e-→Zn2+,故D错误;
故选B.
点评:本题考查了原电池和电解池原理,明确原电池和电解池区别是解本题关键,注意各个电极上得失电子,电极反应式的书写是学习难点,难度中等.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目