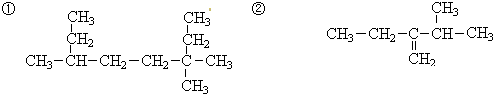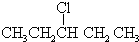题目内容
某恒温密闭容器中,可逆反应A(s)?B+C(g)△H=+Q,达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A、B的状态可能为气态 |
| B、保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动 |
| C、平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1 |
| D、若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、若B为气体,因容器保持恒温,缩小容器体积,达到新平衡时平衡常数不变,则气体C的浓度也一定不变;
B、依据A分析可知B为非气体,加入B平衡不动;
C、平衡时,各物质的量不再改变,正反应速率和逆反应速率相等,因此单位时间内n(A)消耗=n(C)消耗;
D、因反应为可逆反应,故加入1molB和1molC至反应达到平衡时不能完全消耗,放出热量小于Q;
B、依据A分析可知B为非气体,加入B平衡不动;
C、平衡时,各物质的量不再改变,正反应速率和逆反应速率相等,因此单位时间内n(A)消耗=n(C)消耗;
D、因反应为可逆反应,故加入1molB和1molC至反应达到平衡时不能完全消耗,放出热量小于Q;
解答:
解:达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等;
A、若B为气体,因容器保持恒温,缩小容器体积,达到新平衡时平衡常数不变,则气体C的浓度也一定不变;若B是非气体,平衡常数K=c(C),由于C(g)的浓度不变,因此B可以是气体或是非气体,故A正确;
B、根据A的分析判断可知,B为气体,加入后平衡逆向进行,C的浓度改变,B为非气体,则向平衡体系中加入B,平衡不移动,C浓度不变,故B错误;
C、平衡时,各物质的量不再改变,正反应速率和逆反应速率相等,因此单位时间内n(A)消耗=n(C)消耗,C浓度不变,故C正确;
D、因反应为可逆反应,故加入1molB和1molC至反应达到平衡时转化率一定小于100%,因此放出热量小于Q,故D错误;
故选AC.
A、若B为气体,因容器保持恒温,缩小容器体积,达到新平衡时平衡常数不变,则气体C的浓度也一定不变;若B是非气体,平衡常数K=c(C),由于C(g)的浓度不变,因此B可以是气体或是非气体,故A正确;
B、根据A的分析判断可知,B为气体,加入后平衡逆向进行,C的浓度改变,B为非气体,则向平衡体系中加入B,平衡不移动,C浓度不变,故B错误;
C、平衡时,各物质的量不再改变,正反应速率和逆反应速率相等,因此单位时间内n(A)消耗=n(C)消耗,C浓度不变,故C正确;
D、因反应为可逆反应,故加入1molB和1molC至反应达到平衡时转化率一定小于100%,因此放出热量小于Q,故D错误;
故选AC.
点评:本题考查化学平衡影响因素的分析判断,化学判断移动原理的理解设计解题关键,题目难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、反应:2CO(g)+2NO(g)?N2(g)+2CO2(g)在温度为298K时能自发进行,则它的△H>0,△S>0 |
| B、0.1mol/L NH4Cl溶液加蒸馏水稀释,溶液的pH不断减小 |
| C、为保护浸入海水中的钢闸门,可在闸门表面镶上铜锭 |
| D、反应:2A(g)?B(g)+2C(g),增大压强反应速率加快,A的转化率减小 |
某无色溶液中放人铝片后有氢气产生,则下列离子在该溶液中肯定可以大量存在的是( )
| A、Na+ |
| B、Mg2+ |
| C、OH- |
| D、HCO3- |
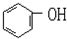
下列有机物的命名正确的是( )
A、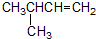 2-甲基-3-丁烯 2-甲基-3-丁烯 |
B、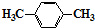 对甲二苯 对甲二苯 |
C、 2-乙基丙烷 2-乙基丙烷 |
| D、CH3CH2CH2CH2OH 1-丁醇 |
下列叙述正确的是( )
| A、离子晶体中,只存在离子键,不可能存在其他化学键 |
| B、在卤族元素(F、Cl、Br、I)的氢化物中,HF的沸点最低 |
| C、NaHSO4、Na2O2晶体中的阴、阳离子个数比均为1:1 |
| D、晶体熔点:金刚石>食盐>冰>干冰 |