题目内容
能正确表示下列反应的离子方程式的是( )
| A、向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2 H++SO42-=BaSO4↓+2H2O |
| B、用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、NH4HCO3溶于过量的KOH溶液中:HCO3-+OH-═CO32-+H2O |
| D、等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成硫酸钡和水;
B.醋酸是弱电解质,写化学式;
C.二者反应生成一水合氨和碳酸根离子、水;
D.反应生成氢氧化镁、水.
B.醋酸是弱电解质,写化学式;
C.二者反应生成一水合氨和碳酸根离子、水;
D.反应生成氢氧化镁、水.
解答:
解:A.二者反应生成硫酸钡和水,离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A正确;
B.醋酸是弱电解质,写化学式,离子方程式为CaCO3+2CH3COOH═Ca2++CO2↑+H2O+2CH3COO-,故B错误;
C.二者反应生成一水合氨和碳酸根离子、水,离子方程式为NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O,故C错误;
D.反应生成氢氧化镁、水,离子方程式为2H++Mg2++4OH-═Mg(OH)2↓+2H2O,故D错误;
故选A.
B.醋酸是弱电解质,写化学式,离子方程式为CaCO3+2CH3COOH═Ca2++CO2↑+H2O+2CH3COO-,故B错误;
C.二者反应生成一水合氨和碳酸根离子、水,离子方程式为NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O,故C错误;
D.反应生成氢氧化镁、水,离子方程式为2H++Mg2++4OH-═Mg(OH)2↓+2H2O,故D错误;
故选A.
点评:本题考查离子方程式的书写,为高考高频点,明确物质性质及离子方程式书写规则是解本题关键,注意D中离子反应先后顺序,为易错点.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
现有2mol/L稀硫酸30mL,往其中加入1.7gNaNO3晶体,充分溶解,该混和液最多可溶解铜的物质的量为( )
| A、0.03mol |
| B、0.045mol |
| C、0.0225mol |
| D、0mol |
下列化学用语或模型表示正确的是( )
A、硝基苯的结构简式: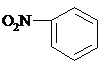 |
B、COCl2分子的电子式: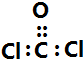 |
C、过氧化氢的电子式: |
D、NaCl的晶体模型: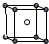 |
2011年3月11日日本发生9.0级的强震并引发海啸和核泄露,核电站周围检测到放射性物质碘131,下列有关说法正确的是( )
| A、核裂变是一种化学变化 |
| B、131I 与127I互为同素异形体 |
| C、131I 原子的中子数为78 |
| D、碘在周期表中位于第四周期ⅦA族 |
有关Na2CO3和NaHCO3的叙述中正确的是( )
| A、相同质量的Na2CO3和NaHCO3与足量盐酸作用时,碳酸氢钠反应速率更快,产生的气体质量相同 |
| B、NaHCO3俗名:小苏打.Na2CO3俗名:大苏打 |
| C、Na2CO3和NaHCO3均可与澄清石灰水反应 |
| D、Na2CO3和NaHCO3均可与NaOH溶液反应 |
下列有关实验操作的说法错误的是( )
| A、中和滴定时盛待测液的锥形瓶中有少量水对滴定结果无影响 |
| B、在酸碱中和滴定实验中,滴定管都需润洗,否则引起误差 |
| C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
| D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
 “中国水周”活动的宣传主题为“大力加强农田水利,保障国家粮食安全”.
“中国水周”活动的宣传主题为“大力加强农田水利,保障国家粮食安全”.