题目内容
10.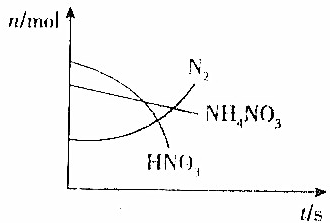 某容器中发生一个化学反应,反应过程中存在Zn、H2O、HNO3、N2、NH4NO3和Zn(NO3)2六种物质,在反应过程中测得HNO3、NH4NO3和N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )
某容器中发生一个化学反应,反应过程中存在Zn、H2O、HNO3、N2、NH4NO3和Zn(NO3)2六种物质,在反应过程中测得HNO3、NH4NO3和N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )| A. | N2是还原产物,Zn(NO3)2是氧化产物 | |
| B. | NH4NO3是氧化剂,Zn是还原剂 | |
| C. | 反应生成1molN2时共有5mol电子转移 | |
| D. | HNO3在反应中没有表现出酸性 |
分析 由图可知HNO3、NH4NO3的物质的量减少是反应物,所以反应方程式为:Zn+2HNO3+NH4NO3=N2↑+Zn(NO3)2+3H2O中,Zn元素的化合价由0升高为+2价,N元素的化合价既升高又降低,以此来解答.
解答 解:由图可知HNO3、NH4NO3的物质的量减少是反应物,所以反应方程式为:Zn+2HNO3+NH4NO3=N2↑+Zn(NO3)2+3H2O中,Zn元素的化合价由0升高为+2价,N元素的化合价既升高又降低,
A.N2是还原产物也是氧化产物,Zn(NO3)2只是氧化产物,故A错误;
B.NH4NO3是还原剂,Zn是还原剂,故B错误;
C.由硝酸中N元素的化合价变化可知,反应中生成1 molN2时共有5mol电子发生转移,故C正确;
D.HNO3在反应中生成硝酸锌,表现出酸性,故D错误;
故选C.
点评 本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,侧重氧化还原反应中的基本概念、转移电子数的考查,题目难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
18.制造下列文化用品的原料不属于有机材料的是( )
| A. | 纸 | B. | 铅笔芯 | C. | 塑料文具盒 | D. | 橡皮擦 |
5.X元素的原子序数是9,下列哪一原子序数的元素与X具有相似的化学性质( )
| A. | 1 | B. | 8 | C. | 17 | D. | 18 |
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温下,44gCO2含有NA个C原子 | |
| B. | 1 L0.1mol•L-1Na2S溶液中含有0.1NA个S2- | |
| C. | 0.1mol Na与足量O2反应,转移0.2NA个电子 | |
| D. | 标准状况下,22.4L的CCl4含有4NA个Cl原子 |
20.重铬酸钠(Na2Cr2O7•2H2O)俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿(主要成份为FeO•Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如图:

①中涉及的主要反应有:
主反应:4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;\;△\;\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2SiO3+CO2↑、Al2O3+Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
试回答下列问题:
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是使反应物接触更充分,加快反应速率.
(2)“③”中调节pH至4.7,目的是除去溶液中的AlO2-、SiO32-.
(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式:2CrO42-+2H+?Cr2O72-+H2O.
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol•L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol•L-1Na2S2O3标准溶液滴定(I2+2S2O32-═2I-+S4O62-).
①判断达到滴定终点的依据是:当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色;
②若实验中共用去Na2S2O3标准溶液40.00ml,所得产品的中重铬酸钠的纯度(设整个过程中其它杂质不参与反应)83.84%.

①中涉及的主要反应有:
主反应:4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;\;△\;\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2SiO3+CO2↑、Al2O3+Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| 完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是使反应物接触更充分,加快反应速率.
(2)“③”中调节pH至4.7,目的是除去溶液中的AlO2-、SiO32-.
(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式:2CrO42-+2H+?Cr2O72-+H2O.
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol•L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol•L-1Na2S2O3标准溶液滴定(I2+2S2O32-═2I-+S4O62-).
①判断达到滴定终点的依据是:当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色;
②若实验中共用去Na2S2O3标准溶液40.00ml,所得产品的中重铬酸钠的纯度(设整个过程中其它杂质不参与反应)83.84%.
1.下列说法正确的是( )
| A. | 漂白粉的有效成份是氯酸钙 | B. | 氟化氢溶于水形成的氢氟酸是强酸 | ||
| C. | 碘化钾水溶液能使淀粉变蓝 | D. | 氟气通入水中有氧气生成 |
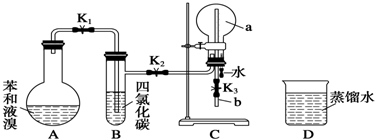
 ,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.
,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.