题目内容
13.A元素原子得电子变成阴离子释放出的能量比B元素原子得电子变成阴离子释放出的能量大,则( )| A. | 氧化性A->B- | B. | 还原性 A->B- | C. | 氧化性 A>B | D. | 还原性A>B |
分析 A与B两种元素的原子,当它们分别获得电子形成稳定结构的阴离子,A放出的能量大于B,说明A的非金属性大于B,结合主族元素性质的递变规律解答该题.
解答 解:A与B两种元素的原子,当它们分别获得电子形成稳定结构的阴离子,A放出的能量大于B,说明A的非金属性大于B,元素的非金属性越强,其单质的氧化性越强,其阴离子的还原性越弱,所以氧化性A>B,还原性 A-<B-,
故C正确;
故选C.
点评 本题考查原子的结构与元素的性质、氧化还原反应,题目难度中等,注意从能量的角度判断元素的性质为解答该题的关键,侧重于考查学生的分析能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.已知在一定条件下,二个氨基酸分子之间失去一分子水,缩合生成“二肽”.现将甘氨酸[CH2(NH2)-COOH]和丙氨酸[CH3-CH(NH2)-COOH]组成的混合物,在一定条件下发生缩合反应,生成的“二肽”可能有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
1.实验室制Cl2的反应如下:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,下列有关该反应的说法正确的是( )
| A. | MnO2是还原剂 | B. | HCl被氧化 | ||
| C. | MnO2发生氧化反应 | D. | 每反应4molHCl转移4mol电子 |
8.下列有关化学用语能确定为丙烯的是( )
| A. |  | B. | C3H6 | C. |  | D. | CH2CHCH3 |
18.下列各醇,能发生催化氧化的是( )
| A. | 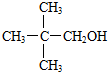 | B. |  | C. | 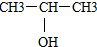 | D. | 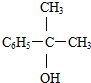 |
5.1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
| A. | Na2CO3、Na2O2 | B. | Na2CO3 | ||
| C. | NaOH、Na2CO3 | D. | Na2O2、NaOH、Na2CO3 |
3.将气体A、B置于容积为2L的密闭容器中,发生如下反应:4A(g)+B(g)═2C(g),反应进行到4s末,测得A为0.5mol,B为0.4mol,C为0.2mol.用反应物A浓度的减少来表示该反应的速率应为( )
| A. | 0.025mol•L-1•s-1 | B. | 0.0125mol•L-1•s-1 | ||
| C. | 0.05mol•L-1•s-1 | D. | 0.1mol•L-1•s-1 |
 现有一瓶葡萄糖(C6H12O6)溶液,部分标签如右表所示,请计算(本题只要求写出计算结果):
现有一瓶葡萄糖(C6H12O6)溶液,部分标签如右表所示,请计算(本题只要求写出计算结果):