题目内容
下列离子方程式正确的是( )
| A、钠投入水中:Na+H2O=Na++OH-+H2↑ |
| B、HCl溶液与NaOH溶液反应:H++OH-=H2O |
| C、石灰石溶于盐酸中:CO32-+H+=CO2↑+H2O |
| D、Zn与H2SO4溶液反应:Zn+2H+=Zn2++H2↑ |
考点:离子方程式的书写
专题:
分析:A.钠与水反应生成氢氧化钠和氢气,离子方程式两边质量不守恒;
B.氯化氢与氢氧化钠为可溶性的酸碱溶液,反应生成了可溶性的氯化钠;
C.石灰石为碳酸钙,碳酸钙为难溶物,在离子方程式中应该保留化学式,离子方程式两边氢原子不守恒;
D.金属锌与稀硫酸溶液反应生成硫酸锌和氢气,锌与浓硫酸反应产物不是氢气,所以必须指出浓硫酸还是稀硫酸.
B.氯化氢与氢氧化钠为可溶性的酸碱溶液,反应生成了可溶性的氯化钠;
C.石灰石为碳酸钙,碳酸钙为难溶物,在离子方程式中应该保留化学式,离子方程式两边氢原子不守恒;
D.金属锌与稀硫酸溶液反应生成硫酸锌和氢气,锌与浓硫酸反应产物不是氢气,所以必须指出浓硫酸还是稀硫酸.
解答:
解:A.钠与水反应生成氢氧化钠和氢气,离子方程式两边质量不相等,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B.HCl溶液与NaOH溶液反应生成氯化钠和水,反应的离子方程式为:H++OH-=H2O,故B正确;
C.碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,其反应的离子方程式为:CaCO3+2H+=CO2↑+H2O+Ca2+,故C错误;
D.Zn与稀H2SO4溶液反应生成氢气,反应的离子方程式为:Zn+2H+=Zn2++H2↑,但是锌与浓硫酸反应生成产物不是氢气,必须指出是浓硫酸还是稀硫酸,故D错误;
故选B.
B.HCl溶液与NaOH溶液反应生成氯化钠和水,反应的离子方程式为:H++OH-=H2O,故B正确;
C.碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,其反应的离子方程式为:CaCO3+2H+=CO2↑+H2O+Ca2+,故C错误;
D.Zn与稀H2SO4溶液反应生成氢气,反应的离子方程式为:Zn+2H+=Zn2++H2↑,但是锌与浓硫酸反应生成产物不是氢气,必须指出是浓硫酸还是稀硫酸,故D错误;
故选B.
点评:本题考查了离子方程式的书写判断,难度中等,注意掌握离子方程式的正确书写方法,熟悉常见的难溶物、弱电解质、气体等物质,选项D为易错点,注意锌与浓硫酸和稀硫酸反应产物不同.

练习册系列答案
相关题目
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )


| A、加入Na2SO4可使溶液由a点变到b点 |
| B、通过蒸发可以使溶液由d点变到c点 |
| C、b点有BaSO4沉淀生成 |
| D、a点对应的Ksp大于c点对应的Ksp |
某铁的氧化物样品,用50mL2mol/L的盐酸恰好完全溶解,若所得溶液吸收标准状况下Cl2224ml,可以使溶液中的亚铁离子全部转化为三价铁离子.则该样品可能的化学式是( )
| A、FeO |
| B、Fe3O4 |
| C、Fe4O5 |
| D、Fe5O7 |
下列装置属于原电池的是 ( )
A、 |
B、 |
C、 |
D、 |
下列表示物质结构的化学用语或模型正确的是( )
A、TNT的结构简式为: |
B、苯乙醛的结构简式为: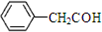 |
C、丙烷分子的球棍模型为: |
| D、乙烯的结构简式为:CH2CH2 |

