题目内容
3.写出下列物质或微粒的电子式(1)硫离子
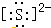
(2)CO2

(3)KOH

(4)N2
 .
.
分析 (1)硫离子为阴离子,需要标出最外层电子及所带电荷;
(2)CO2是共价化合物,碳原子和氧原子之间有2对电子;
(3)氢氧化钾为离子化合物,电子式需要标出阴阳离子所带电荷;
(4)氮气分子中存在氮氮三键,氮原子最外层均达到8电子稳定结构;
解答 解:(1)硫离子为阴离子,需要标出最外层8个电子,硫离子的电子式为: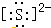 ,故答案为:
,故答案为: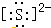 ;
;
(2)CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,故答案为:
,故答案为: ;
;
(3)氢氧化钾为离子化合物,由钾离子和氢氧根离子构成,氢氧化钾的电子式为: ,
,
故答案为: ;
;
(4)N2中两个N原子间为氮氮三键,氮原子最外层均达到8电子稳定结构,故氮气的电子式为: ,故答案为:
,故答案为:
点评 本题考查了电子式的书写,题目难度中等,注意掌握电子式的概念及表示方法,明确离子化合物与共价化合物的电子式的表示方法及区别.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
13.下列电子式正确的是( )
| A. | 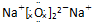 | B. | 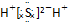 | C. | 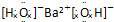 | D. | 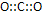 |
18.2005年2月18日英国食品标准署就食用含有添加苏丹红色素的食品可能诱发癌症向消费者发出警告.我国也已开始追查含苏丹红色素的食品.所谓“苏丹红一号”实际上一般称为“苏丹一号”,是一种黄溶剂染料,按化学染料分类称为溶剂黄14(C.L.Solvent,Yellow14),分子式为C16H12N2O,其化学结构属偶氮类染料.有关苏丹红一号下列说法正确的是( )
| A. | 苏丹红一号在食品中能起到增色的作用,可在辣椒酱中用作添加剂 | |
| B. | 苏丹红一号的摩尔质量为248 | |
| C. | 苏丹红一号可用于溶解剂、机油、蜡和鞋油等产品的染色 | |
| D. | 食品添加剂对人体危害较大,因此应全面禁止使用 |
8.下列关于仪器使用的说法正确的是( )
| A. | 用四氯化碳萃取碘单质,静置,上层显示紫红色 | |
| B. | 坩埚需要垫石棉网加热 | |
| C. | 蒸馏时温度计水银球可以高于蒸馏烧瓶支管口 | |
| D. | 蒸发时用玻璃棒和向容量瓶移液时用玻璃棒用途不同 |
12.在一密闭容器中,一定条件下发生反应A+3B?2C,在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则用B浓度的变化表示的该反应在这段时间内的平均反应速率为( )
| A. | 0.04 mol/(L•s) | B. | 0.12 mol/(L•s) | C. | 0.4 mol/(L•s) | D. | 1.2 mol/(L•s) |
 .
.