题目内容
已知X、Y、Z、U、V、W是短周期内的六种元素,它们的原子序数依次增大.X元素原子形成的离子就是一个质子,Y元素的一种同素异形体在自然界中硬度最大,U、Z在元素周期表中处于相邻位置,它们的单质在常温下均为无色气体,V元素原子半径在短周期元素原子半径中最大,W元素的最高正价与最低负价的代数和为4.
(1)请写出W原子的结构示意图 ;
(2)W单质与Z单质的反应产物在一定条件下与Z单质反应,该反应的化学方程式: .
(3)X、Y、Z、W四种元素组成原子个数比为8:2:4:1的化合物,该化合物的化学式为 .
(4)Z元素的最高价氧化物对应的水化物与Z元素的氢化物可以反应,写出该反应的化学方程式 .
(5)写出Y的最高价氧化物的结构式 .
(6)写出Z、V形成的原子个最比为1:1的化合物的电子式 .
(7)指出Y、Z、U形成氢化物的稳定性由弱到强的顺序: .(用化学式表示)
(1)请写出W原子的结构示意图
(2)W单质与Z单质的反应产物在一定条件下与Z单质反应,该反应的化学方程式:
(3)X、Y、Z、W四种元素组成原子个数比为8:2:4:1的化合物,该化合物的化学式为
(4)Z元素的最高价氧化物对应的水化物与Z元素的氢化物可以反应,写出该反应的化学方程式
(5)写出Y的最高价氧化物的结构式
(6)写出Z、V形成的原子个最比为1:1的化合物的电子式
(7)指出Y、Z、U形成氢化物的稳定性由弱到强的顺序:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、U、V、W是短周期内的六种元素,它们的原子序数依次增大.X元素原子形成的离子就是一个质子,则X为H;Y元素的一种同素异形体在自然界中硬度最大,则Y为C;V元素原子半径在短周期元素原子半径中最大,则V为Na;U、Z在元素周期表中处于相邻位置,它们的单质在常温下均为无色气体,则U为N,Z为O;W元素的最高正价与最低负价的代数和为4,W的最高正价为+6价,为S元素,以此来解答.
解答:
解:X、Y、Z、U、V、W是短周期内的六种元素,它们的原子序数依次增大.X元素原子形成的离子就是一个质子,则X为H;Y元素的一种同素异形体在自然界中硬度最大,则Y为C;V元素原子半径在短周期元素原子半径中最大,则V为Na;U、Z在元素周期表中处于相邻位置,它们的单质在常温下均为无色气体,则U为N,Z为O;W元素的最高正价与最低负价的代数和为4,W的最高正价为+6价,为S元素,
(1)W为S,原子结构示意图为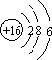 ,故答案为:
,故答案为: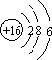 ;
;
(2)W单质与Z单质的反应产物在一定条件下与Z单质反应,为二氧化硫的催化氧化反应,该反应为2SO2+O2
2SO3,故答案为:2SO2+O2
2SO3;
(3)X、Y、Z、W四种元素组成原子个数比为8:2:4:1的化合物为(NH4)2SO4,故答案为:(NH4)2SO4;
(4)Z元素的最高价氧化物对应的水化物为硝酸,与Z元素的氢化物氨气反应生成硝酸铵,该反应为NH3+HNO3═NH4NO3,故答案为:NH3+HNO3═NH4NO3;
(5)Y的最高价氧化物为二氧化碳,其结构式为O=C=O,故答案为:O=C=O;
(6)Z、V形成的原子个最比为1:1的化合物为Na2O2,其电子式为Na+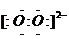 Na+,故答案为:Na+
Na+,故答案为:Na+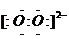 Na+;
Na+;
(7)非金属C<N<O,则Y、Z、U形成氢化物的稳定性由弱到强的顺序为CH4<NH3<H2O,故答案为:CH4<NH3<H2O.
(1)W为S,原子结构示意图为
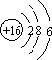 ,故答案为:
,故答案为: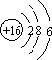 ;
;(2)W单质与Z单质的反应产物在一定条件下与Z单质反应,为二氧化硫的催化氧化反应,该反应为2SO2+O2
| 催化剂 |
| △ |
| 催化剂 |
| △ |
(3)X、Y、Z、W四种元素组成原子个数比为8:2:4:1的化合物为(NH4)2SO4,故答案为:(NH4)2SO4;
(4)Z元素的最高价氧化物对应的水化物为硝酸,与Z元素的氢化物氨气反应生成硝酸铵,该反应为NH3+HNO3═NH4NO3,故答案为:NH3+HNO3═NH4NO3;
(5)Y的最高价氧化物为二氧化碳,其结构式为O=C=O,故答案为:O=C=O;
(6)Z、V形成的原子个最比为1:1的化合物为Na2O2,其电子式为Na+
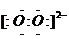 Na+,故答案为:Na+
Na+,故答案为:Na+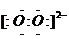 Na+;
Na+;(7)非金属C<N<O,则Y、Z、U形成氢化物的稳定性由弱到强的顺序为CH4<NH3<H2O,故答案为:CH4<NH3<H2O.
点评:本题考查位置、结构、性质的关系及应用,为高频考点,把握元素及化合物的性质、原子结构推断元素为解答的关键,侧重分析与推断能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列判断错误的是( )
| A、熔点:金刚石>碳化硅>晶体硅 |
| B、沸点:NH3>PH3>AsH3 |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
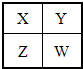 已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法不正确的是( )
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法不正确的是( )| A、Y原子形成的简单离子半径一定比X原子形成的简单离子半径大 |
| B、W的原子序数可能是Y的原子序数的3倍 |
| C、Y的气态氢化物的稳定性一定比W的强 |
| D、若Z元素最高价氧化物的水化物是强酸,则W元素的单质具有强氧化性 |
①1mol某链烃最多能和2mol HCl发生加成反应,生成1mol氯代烷;②1mol该氯代烷能和8mol Cl2发生取代反应,生成只含碳元素和氯元素的氯代烃.该链烃可能是( )
| A、CH3CH═CH2 |
| B、CH2═CHCH═CH2 |
| C、CH3CH═CHCH3 |
| D、CH3C≡CH |