题目内容
原子序数为1-18号的元素中,下列叙述正确的是( )
| A、最外层只有1个电子的元素一定是金属元素 |
| B、最外层只有2个电子的元素一定是金属元素 |
| C、原子核外各层电子数相等的元素不一定是金属元素 |
| D、核电荷数为17的元素的原子在化学反应中容易得到1个电子 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.最外层只有一个电子的元素可能是非金属元素;
B.最外层只有2个电子的元素可能是非金属元素;
C.原子核外各层电子数相等的元素可能是金属元素;
D.核电荷数为17的元素是Cl元素,其最外层有7个电子,在反应中易得电子.
B.最外层只有2个电子的元素可能是非金属元素;
C.原子核外各层电子数相等的元素可能是金属元素;
D.核电荷数为17的元素是Cl元素,其最外层有7个电子,在反应中易得电子.
解答:
解:A.最外层只有一个电子的元素可能是非金属元素,如H元素,故A错误;
B.最外层只有2个电子的元素可能是非金属元素,如He元素,故B错误;
C.原子核外各层电子数相等的元素可能是金属元素,如Be元素,故C错误;
D.核电荷数为17的元素是Cl元素,其最外层有7个电子,在反应中易得1个电子使最外层达到8电子稳定结构,故D正确;
故选D.
B.最外层只有2个电子的元素可能是非金属元素,如He元素,故B错误;
C.原子核外各层电子数相等的元素可能是金属元素,如Be元素,故C错误;
D.核电荷数为17的元素是Cl元素,其最外层有7个电子,在反应中易得1个电子使最外层达到8电子稳定结构,故D正确;
故选D.
点评:本题考查了元素原子结构和元素周期表,根据原子结构确定元素,会利用反例法分析解答,题目难度不大.

练习册系列答案
相关题目
50mL 0.1mol/L FeCl3溶液与25mL 0.2mol/L KCl溶液中的Cl-的数目之比( )
| A、5:2 | B、3:1 |
| C、2:5 | D、1:3 |
丁腈橡胶-[CH2-CH=CH-CH2-CH2-CH]-CNn具有优良的耐油,耐高温的性能,合成丁腈橡胶的原料是( )
(1)CH2=CH-CH=CH2 (2)CH3-CC-CH3 (3)CH2=CH-CN
(4)CH2-CH=CH-CN (5)CH3-CH=CH2 (6)CH3-CH=CH-CH3.
(1)CH2=CH-CH=CH2 (2)CH3-CC-CH3 (3)CH2=CH-CN
(4)CH2-CH=CH-CN (5)CH3-CH=CH2 (6)CH3-CH=CH-CH3.
| A、(1)(3) |
| B、(2)(3) |
| C、(3)(6) |
| D、(4)(5) |
20mL 0.1mol/L溶液中含有Fe2+,向其中滴加NaOH溶液至pH=4,溶液中有沉淀生成,过滤,得沉淀和滤液.已知:Kaq=[Fe(OH)3]=4.0×10-38,Kaq=[Fe(OH)2]=8.0×10-16.( )
| A、沉淀中只有Fe(OH)3 |
| B、沉淀中有Fe(OH)3和Fe(OH)2 |
| C、滤液c(Fe3+)=4.0×10-8mol/L |
| D、向滤液中滴加FeCl2溶液,无沉淀产生 |
下列各组离子中,全组离子均与氖原子电子层结构相同的是( )
| A、Na+、Mg2+、Al3+、O2-、F- |
| B、Li+、Na+、F-、O2-、Cl- |
| C、Na+、Mg2+、Al3+、K+、Ca2+ |
| D、S2-、Cl-、K+、Ca2+、Na+ |
下列离子方程式正确的是( )
| A、氨水与盐酸反应:H++OH-═H2O |
| B、锌与稀醋酸反应:Zn+2H+═Zn2++H2↑ |
| C、碳酸钙与硝酸反应:CO32-+2H+═CO2↑+H2O |
| D、氯气与水反应:Cl2+H2O═H++Cl-+HClO |
合成氨工业生产中所用的α-Fe催化剂的成分是FeO、Fe2O3,当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化活性最高,此时混合物中铁的质量分数约为( )
| A、70.0% |
| B、77.8% |
| C、72.4% |
| D、75.0% |
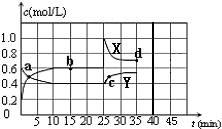 已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.请回答:
已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.请回答: