题目内容
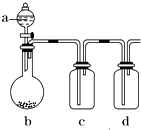 有几个实验小组的同学,利用右图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.
有几个实验小组的同学,利用右图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.请你回答以下各组同学在交流实验设计方案中提出的问题:
Ⅰ.(1)若a:浓盐酸;b:高锰酸钾(其氧化性比二氧化锰强很多);c:红色鲜花瓣.在实验过程中c中的现象
(2)若a:稀盐酸;b:贝壳粉;c:饱和碳酸钠溶液;d:饱和Na2SiO3溶液.在实验过程中,c中出现的现象是
Ⅱ.你认为四组同学在制取气体之前都应进行的操作是
考点:实验装置综合
专题:实验设计题
分析:Ⅰ.(1)高锰酸钾和浓盐酸反应生成氯气,氯气可使鲜花褪色,可与氢氧化钠反应;
(2)稀盐酸和贝壳粉反应生成二氧化碳气体,用饱和碳酸氢钠可除去氯化氢,二氧化碳与硅酸钠反应生成硅酸;
Ⅱ.制备气体,应首先检验气密性,装置适用于固体和液体在不加热条件下生成气体的反应.
(2)稀盐酸和贝壳粉反应生成二氧化碳气体,用饱和碳酸氢钠可除去氯化氢,二氧化碳与硅酸钠反应生成硅酸;
Ⅱ.制备气体,应首先检验气密性,装置适用于固体和液体在不加热条件下生成气体的反应.
解答:
解:Ⅰ.(1)高锰酸钾和浓盐酸反应生成氯气,氯气与水反应生成具有漂白性的次氯酸,氯气可使鲜花褪色,由于氯气有毒,不能排放到空气中,且与氢氧化钠反应,则可用氢氧化钠溶液进行尾气吸收,反应的离子方程式为Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:花瓣褪色;吸收未反应的氯气,防止污染空气;Cl2+2OH-═Cl-+ClO-+H2O;
(2)稀盐酸和贝壳粉反应生成二氧化碳气体,用饱和碳酸氢钠可除去氯化氢,由于碳酸酸性比硅酸强,二氧化碳与硅酸钠反应生成硅酸,可观察到胶状物质生成,
故答案为:有白色沉淀析出;出现胶状物质;生成不溶性的硅酸,即硅酸的酸性弱于碳酸;
Ⅱ.气体制备之前需检查气密性,此装置适合固液或液液不加热制气装置,可用于制备氧气(或二氧化硫),
故答案为:装置气密性检查;氧气(或二氧化硫).
故答案为:花瓣褪色;吸收未反应的氯气,防止污染空气;Cl2+2OH-═Cl-+ClO-+H2O;
(2)稀盐酸和贝壳粉反应生成二氧化碳气体,用饱和碳酸氢钠可除去氯化氢,由于碳酸酸性比硅酸强,二氧化碳与硅酸钠反应生成硅酸,可观察到胶状物质生成,
故答案为:有白色沉淀析出;出现胶状物质;生成不溶性的硅酸,即硅酸的酸性弱于碳酸;
Ⅱ.气体制备之前需检查气密性,此装置适合固液或液液不加热制气装置,可用于制备氧气(或二氧化硫),
故答案为:装置气密性检查;氧气(或二氧化硫).
点评:本题考查了气体的制备和气体性质的检验,为高频考点,侧重于学生的分析能力和实验能力的考查,要明确实验目的,结合实验原理和气体的性质准确回答实验现象和结论,难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
下列叙述中正确的是( )
| A、NH3、CO、CO2都是极性分子 |
| B、CH4、CO2都是含有极性键的非极性分子 |
| C、HF、HCl、HBr的沸点依次增强 |
| D、CS2、H2O、C2H2都是直线型分子 |
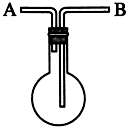 利用如图装置收集以下7种气体:(填气体序号或A或B)
利用如图装置收集以下7种气体:(填气体序号或A或B)