题目内容
K2CO3、KHCO3混合粉末m g,在加热到质量不再减少为止,剩余物质为n g.
(1)则混合物中K2CO3的质量为 .
(2)题干条件中n的数值应满足的范围是 <n<m.
(3)如果将该加热前的K2CO3、KHCO3混合粉末与足量盐酸反应,所得溶液蒸发至干,可得KCl固体 g.
(1)则混合物中K2CO3的质量为
(2)题干条件中n的数值应满足的范围是
(3)如果将该加热前的K2CO3、KHCO3混合粉末与足量盐酸反应,所得溶液蒸发至干,可得KCl固体
考点:有关混合物反应的计算
专题:计算题
分析:(1)加热发生反应2KHCO3
K2CO3+CO2↑+H2O,导致固体质量减少,利用差量法计算KHCO3的质量,进而计算K2CO3的质量;
(2)当mg全部为KHCO3时,加热分解后,剩余固体的质量最小,根据方程式计算;
(3)K2CO3、KHCO3混合物中钾离子物质的量等于ng碳酸钾中钾离子的物质的量,根据K元素守恒计算n(KCl),再根据m=nM计算KCl的质量.
| ||
(2)当mg全部为KHCO3时,加热分解后,剩余固体的质量最小,根据方程式计算;
(3)K2CO3、KHCO3混合物中钾离子物质的量等于ng碳酸钾中钾离子的物质的量,根据K元素守恒计算n(KCl),再根据m=nM计算KCl的质量.
解答:
解:(1)令混合物中KHCO3的质量为a,则:
2KHCO3
K2CO3+CO2↑+H2O 质量减少
200g 62g
a (m-n)g
故a=
=
g
故K2CO3的质量=mg-
g=[m-
]g
故答案为:[m-
]g;
(2)当mg全部为KHCO3时,加热分解后,剩余固体的质量最小,令此时生成碳酸钾的质量为b,则:
2KHCO3
K2CO3+CO2↑+H2O
200g 138g
mg b
故b=
=
g,
故
<n,
故答案为:
;
(3)K2CO3、KHCO3混合物中钾离子物质的量等于ng碳酸钾中钾离子的物质的量,根据K元素守恒,n(KCl)=2×
=
mol,则KCl的质量=
mol×74.5g/mol=
g,故答案为:
.
2KHCO3
| ||
200g 62g
a (m-n)g
故a=
| 200g×(m-n)g |
| 62g |
| 100(m-n) |
| 31 |
故K2CO3的质量=mg-
| 100(m-n) |
| 31 |
| 100(m-n) |
| 31 |
故答案为:[m-
| 100(m-n) |
| 31 |
(2)当mg全部为KHCO3时,加热分解后,剩余固体的质量最小,令此时生成碳酸钾的质量为b,则:
2KHCO3
| ||
200g 138g
mg b
故b=
| mg×138g |
| 200g |
| 69m |
| 100 |
故
| 69m |
| 100 |
故答案为:
| 69m |
| 100 |
(3)K2CO3、KHCO3混合物中钾离子物质的量等于ng碳酸钾中钾离子的物质的量,根据K元素守恒,n(KCl)=2×
| ng |
| 138g/mol |
| n |
| 69 |
| n |
| 69 |
| 149n |
| 138 |
| 149n |
| 138 |
点评:本题考查混合物计算,难度中等,明确发生的反应是关键,注意差量法、极限法与守恒法的应用.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
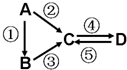 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系: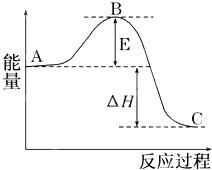 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.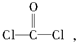 每个COCl2分子内含有
每个COCl2分子内含有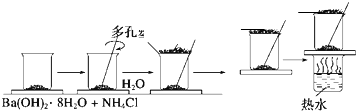 在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20g已研磨成粉末的Ba(OH)2?8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10g NH4Cl晶体,根据实验步骤,填写下表,并回答问题.
在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20g已研磨成粉末的Ba(OH)2?8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10g NH4Cl晶体,根据实验步骤,填写下表,并回答问题.