题目内容
在25°C时,水电离出的c (H+ )为 ,c(OH-)为 .随着温度的升高,c (H+ )会 (填增大、减小或不变).
【答案】分析:常温下,水的离子积Kw=10-14,溶液的PH=7,溶液显示中性,c(H+)=c(OH-)=10-7 mol/L;
水的电离是吸热反应,温度升高,水的电离程度增大,溶液中氢离子、氢氧根浓度增大.
解答:解:在25°C时,Kw=c(H+)?c(OH-)=10-14,溶液显示中性,c(H+)=c(OH-)=10-7 mol/L;
由于水的电离是吸热反应,升高温度,促进了水的电离,溶液中氢离子和氢氧根浓度都增大;
故答案是:10-7 mol/L;10-7 mol/L;增大.
点评:本题考查了水的电离,注重了基础知识的考查,难度较低.
水的电离是吸热反应,温度升高,水的电离程度增大,溶液中氢离子、氢氧根浓度增大.
解答:解:在25°C时,Kw=c(H+)?c(OH-)=10-14,溶液显示中性,c(H+)=c(OH-)=10-7 mol/L;
由于水的电离是吸热反应,升高温度,促进了水的电离,溶液中氢离子和氢氧根浓度都增大;
故答案是:10-7 mol/L;10-7 mol/L;增大.
点评:本题考查了水的电离,注重了基础知识的考查,难度较低.

练习册系列答案
相关题目
氮及其化合物在工农业生产、生活中有者重要作用.请回答下列问题:
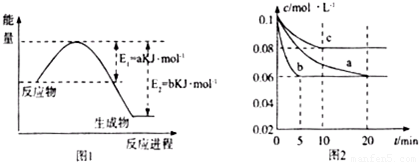
(1)图1是1molNO2和1mol CO反应生成CO2和NO过程中能星变化示意图(a、b均大 于0>,且知:
2CO(g)+2NO(g)=N2(g)+2CO2(g)△H=-ckJ?mol-1(c>0)
请写出CO将NO2还原至N2时的热化学方程式______;
(2)图2是实验室在三个不同条件的密闭容器中合成氨时,N2的浓度随时间的变化曲线(以a、b、c表示).已知三个条件下起始加入浓度均为:c(N2)=0.1mol?L-1,c(H2)=0.3mol?L-1;合成氨的反应:N2(g)+3H2(g)?2NH3(g)△H<0
①计算在a达平衡时H2的转化率为______;
②由图2可知,b、c各有一个条件与a不同,则c的条件改变可能是______;试写出判断b与a条件不同的理由______;
(3)利用图2中c条件下合成氨(容积固定).已知化学平衡常数K与温度(T)的关系如 下表:
①试确定K1的相对大小,K1______4.1x106(填写“>”“-”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据的是______ (填序号字母).
A.容器内NH3的浓度保持不变 B.2v( N2)(正)-v( H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)①NH4Cl溶液呈酸性的原因是(用离子反应方程式表示)______.
②25°C时,将PH=x氨水与pH=y的疏酸(且x+y-14,x>11 )等体积混合后,所得溶液 中各种离子的浓度关系正确的是
A.[SO ]>[NH
]>[NH ]>[H+]>[OH-]
]>[H+]>[OH-]
B.[NH ]>[SO
]>[SO ]>[OH-]>[H+]
]>[OH-]>[H+]
C.[NH ]+[H+]>[SO
]+[H+]>[SO ]+[OH-]
]+[OH-]
D.[NH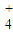 ]>[SO
]>[SO ]>[H+]>[OH-].
]>[H+]>[OH-].

(1)图1是1molNO2和1mol CO反应生成CO2和NO过程中能星变化示意图(a、b均大 于0>,且知:
2CO(g)+2NO(g)=N2(g)+2CO2(g)△H=-ckJ?mol-1(c>0)
请写出CO将NO2还原至N2时的热化学方程式______;
(2)图2是实验室在三个不同条件的密闭容器中合成氨时,N2的浓度随时间的变化曲线(以a、b、c表示).已知三个条件下起始加入浓度均为:c(N2)=0.1mol?L-1,c(H2)=0.3mol?L-1;合成氨的反应:N2(g)+3H2(g)?2NH3(g)△H<0
①计算在a达平衡时H2的转化率为______;
②由图2可知,b、c各有一个条件与a不同,则c的条件改变可能是______;试写出判断b与a条件不同的理由______;
(3)利用图2中c条件下合成氨(容积固定).已知化学平衡常数K与温度(T)的关系如 下表:
| T/(K) | 298 | 398 | 498 | … |
| K/-2 | 4.1×106 | K1 | K2 | … |
②下列各项能作为判断该反应达到化学平衡状态的依据的是______ (填序号字母).
A.容器内NH3的浓度保持不变 B.2v( N2)(正)-v( H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)①NH4Cl溶液呈酸性的原因是(用离子反应方程式表示)______.
②25°C时,将PH=x氨水与pH=y的疏酸(且x+y-14,x>11 )等体积混合后,所得溶液 中各种离子的浓度关系正确的是
A.[SO
 ]>[NH
]>[NH ]>[H+]>[OH-]
]>[H+]>[OH-]B.[NH
 ]>[SO
]>[SO ]>[OH-]>[H+]
]>[OH-]>[H+]C.[NH
 ]+[H+]>[SO
]+[H+]>[SO ]+[OH-]
]+[OH-]D.[NH
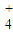 ]>[SO
]>[SO ]>[H+]>[OH-].
]>[H+]>[OH-].
从废钒催化剂(主要成分有V2O5,VOSO4,K2SO4,SiO2等)中回收V2O5的一种生产流程示意图如下,请回答下列问题:
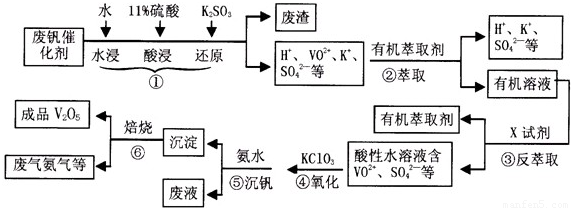
(1)步骤①中废渣的主要成分是______,③中X试剂为______;(均填化学式)
(2)实验室中进行萃取分液操作时,注入萃取剂,充分振荡,将分液漏斗于铁圈上静置,当液体分层后,接下来的操作是______;
(3)②③的变化过程可简化为(下式R表示VO 2+,HA表示有机萃取剂)
R2(SO4)n(水层)+2nHA(有机层)?2RAn(有机层)+nH2SO4(水层)
为提高②中萃取百分率,应采取的措施是______;
(4)请完成④中反应的离子方程式:
______ClO3-+______VO2++______H-+=______VO3++______+______
(5)25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如表
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH值为______;
(6)该工艺流程中,可以循环利用的物质有______.

(1)步骤①中废渣的主要成分是______,③中X试剂为______;(均填化学式)
(2)实验室中进行萃取分液操作时,注入萃取剂,充分振荡,将分液漏斗于铁圈上静置,当液体分层后,接下来的操作是______;
(3)②③的变化过程可简化为(下式R表示VO 2+,HA表示有机萃取剂)
R2(SO4)n(水层)+2nHA(有机层)?2RAn(有机层)+nH2SO4(水层)
为提高②中萃取百分率,应采取的措施是______;
(4)请完成④中反应的离子方程式:
______ClO3-+______VO2++______H-+=______VO3++______+______
(5)25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如表
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
(6)该工艺流程中,可以循环利用的物质有______.
 )+c一定等于
)+c一定等于