题目内容
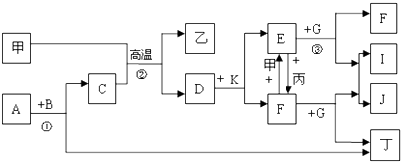
下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液.各物质间的转化如图所示,回答下列各问题(部分生成物未列出):
(1)写出乙的化学式 、甲在周期表中位置是 ;
(2)写出G的一种用途 ;
(3)写出B与K反应的离子方程式: ;
(4)整个转换过程中属于氧化还原反应的有 个;
(5)写出反应③E与G按物质的量之比2:1的反应的离子方程式 .

(1)写出乙的化学式
(2)写出G的一种用途
(3)写出B与K反应的离子方程式:
(4)整个转换过程中属于氧化还原反应的有
(5)写出反应③E与G按物质的量之比2:1的反应的离子方程式
考点:无机物的推断
专题:推断题
分析:D为黑色晶体,应为Fe3O4,J为生活中常见的调味品,应为NaCl,I为红褐色固体,应为Fe(OH)3,甲为常见金属单质,乙、丙、丁是气体单质,可知甲和C的反应应为Fe和水蒸气在高温下的反应,则甲为Fe,C为H2O,乙为H2,由E和F的相互转化可知K应为HCl,E为FeCl2,F为FeCl3,则丙为Cl2,G为淡黄色固体,应为Na2O2,则丁为O2,A为H2O2,B为MnO2,结合对应物质的性质以及题目要求解答该题.
解答:
解:D为黑色晶体,应为Fe3O4,J为生活中常见的调味品,应为NaCl,I为红褐色固体,应为Fe(OH)3,甲为常见金属单质,乙、丙、丁是气体单质,可知甲和C的反应应为Fe和水蒸气在高温下的反应,则甲为Fe,C为H2O,乙为H2,由E和F的相互转化可知K应为HCl,E为FeCl2,F为FeCl3,则丙为Cl2,G为淡黄色固体,应为Na2O2,则丁为O2,A为H2O2,B为MnO2,
(1)由以上分析可知乙为H2,甲为Fe,位于周期表第四周期第Ⅷ族,
故答案为:H2;第四周期第Ⅷ族;
(2)G为Na2O2,可用作供氧剂,
故答案为:供氧剂;
(3)B与K的反应常用于实验室制备氯气,方程式为MnO2+4H++2Cl- =Mn2++Cl2↑+2H2O,
=Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl- =Mn2++Cl2↑+2H2O;
=Mn2++Cl2↑+2H2O;
(4)题中所有反应都涉及氧化还原反应,共6个,
故答案为:6;
(5)反应③FeCl2与Na2O2按物质的量之比2:1的反应,二者恰好发生氧化还原反应,反应的离子方程式为6Fe2++3Na2O2+6H2O=4Fe(OH)3+2Fe3++6Na+,
故答案为:6Fe2++3Na2O2+6H2O=4Fe(OH)3+2Fe3++6Na+.
(1)由以上分析可知乙为H2,甲为Fe,位于周期表第四周期第Ⅷ族,
故答案为:H2;第四周期第Ⅷ族;
(2)G为Na2O2,可用作供氧剂,
故答案为:供氧剂;
(3)B与K的反应常用于实验室制备氯气,方程式为MnO2+4H++2Cl-
 =Mn2++Cl2↑+2H2O,
=Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
 =Mn2++Cl2↑+2H2O;
=Mn2++Cl2↑+2H2O;(4)题中所有反应都涉及氧化还原反应,共6个,
故答案为:6;
(5)反应③FeCl2与Na2O2按物质的量之比2:1的反应,二者恰好发生氧化还原反应,反应的离子方程式为6Fe2++3Na2O2+6H2O=4Fe(OH)3+2Fe3++6Na+,
故答案为:6Fe2++3Na2O2+6H2O=4Fe(OH)3+2Fe3++6Na+.
点评:本题考查无机物的推断,题目难度不大,本题注意根据物质的性质、特征作为突破口进行推断,学习中注意牢固把握元素化合物的性质,不要忽视物质的用途.

练习册系列答案
相关题目
下列溶液加热蒸干后并灼烧,能析出溶质固体的是( )
| A、AlCl3 |
| B、KHCO3 |
| C、Fe2(SO4)3 |
| D、NH4HCO3 |
下列实验现象描述不正确的是( )
| A、钠在空气中燃烧产生黄色火焰,生成淡黄色固体物质 |
| B、新制氯水呈浅黄绿色,氯水放置数天后pH将变大 |
| C、铁与稀盐酸反应生成氯化亚铁,而铁与氯气反应则生成三氯化铁 |
| D、漂白粉的有效成分是次氯酸钙,它具有漂白性是因为在水溶液中生成了有强氧化性的次氯酸 |
已知:CH3OH(g)+
O2(g)═CO2(g)+2H2O(l)△H1△S1
CO(g)+
O2(g)═CO2(g)△H2△S2
H2(g)+
O2(g)═H2O(l)△H3△S3
H2(g)+
O2(g)═H2O(g)△H4△S4
CO(g)+2H2(g)?CH3OH(g)△H5△S5
下列关于上述反应焓变和熵变的判断正确的是( )
| 3 |
| 2 |
CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
CO(g)+2H2(g)?CH3OH(g)△H5△S5
下列关于上述反应焓变和熵变的判断正确的是( )
| A、△H1>0,△S2>0 |
| B、△H3<0,△S3>0 |
| C、△H1+△H5=△H2+△H3 |
| D、△H3<△H4 |
下列有关物质的性质与其应用不相对应的是( )
| A、NaHCO3能与碱反应,食品工业上用作焙制糕点的膨松剂 |
| B、MgO、Al2O3的熔点很高,可制作耐高温材料 |
| C、Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品 |
| D、铜盐能使蛋白质变性,游泳场馆常用硫酸铜作池水消毒剂 |


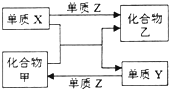 甲、乙是两种常见的化合物,X、Y、Z是三种常见的单质.下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
甲、乙是两种常见的化合物,X、Y、Z是三种常见的单质.下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )