题目内容
15.关于NaHCO3溶液,下列表述不正确的是( )| A. | c (Na+)=c (HCO3-)+c (CO32-)+c (H2CO3) | |
| B. | c(Na+)+c (H+)=c (HCO3-)+c (CO32-)+c (OH-) | |
| C. | HCO3-的水解程度大于HCO3-的电离程度 | |
| D. | c (H+)+c(H2CO3)=c (OH-)+c(CO32-) |
分析 A.碳酸氢钠中存在物料守恒,n(Na)=n(C),碳元素的存在形式之和浓度等于钠离子浓度;
B.溶液中存在电荷守恒分析,阴阳离子所带电荷数相同;
C.碳酸氢钠溶液显碱性;
D.溶液中物料守恒和电荷守恒计算分析判断选项中离子浓度关系;
解答 解:A.碳酸氢钠中存在物料守恒,n(Na)=n(C),c (Na+)=c (HCO3-)+c (CO32-)+c (H2CO3),A正确;
B.溶液中存在电荷守恒,c(Na+)+c (H+)=c (HCO3-)+2c (CO32-)+c (OH-),故B错误;
C.碳酸氢钠是强碱弱酸盐溶液显碱性,HCO3-的水解程度大于HCO3-的电离程度,故C正确;
D.物料守恒c (Na+)=c (HCO3-)+c (CO32-)+c (H2CO3),代入电荷守恒c(Na+)+c (H+)=c (HCO3-)+2c (CO32-)+c (OH-),计算得到c (H+)+c(H2CO3)=c (OH-)+c(CO32-),故D正确;
故选B.
点评 本题考查了盐类水解原理,电解质溶液中物料守恒、电荷守恒等知识,掌握基础是解题关键,题目较简单.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
6.下列物质组合中,既能和酸反应又能和碱反应的化合物是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤(NH4)2CO3.
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤(NH4)2CO3.
| A. | ①②③⑤ | B. | ①②③④⑤ | C. | ①③⑤ | D. | ②③④ |
3.下列说法正确的是( )
| A. | 硫粉在过量的纯氧中燃烧可以生成大量的SO3 | |
| B. | SO2能使品红溶液、酸性KMnO4溶液褪色,褪色原理相同 | |
| C. | 可以用品红溶液鉴别SO2和CO2 | |
| D. | 少量SO2通过CaCl2的溶液能生成白色沉淀 |
20.对于硫酸和硝酸的比较中,下列叙述不正确的是( )
| A. | 冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装 | |
| B. | 金属与浓硫酸或浓硝酸反应都不会产生氢气 | |
| C. | 稀硫酸和稀硝酸都具有氧化性 | |
| D. | 浓硫酸因为有吸水性,可用来干燥HCl、SO2、NH3等多种气体 |
7.下列物质的鉴别方法不正确的是( )
| A. | 用焰色反应鉴别NaCl、KCl | |
| B. | 不用任何试剂可鉴别AlCl3溶液、FeCl3溶液、FeCl2溶液、NaOH溶液CuSO4溶液 | |
| C. | 向某溶液中加入NaOH溶液,加热,用蓝色石蕊试纸检验产生的气体,若试纸变红,则溶液中含有NH${\;}_{4}^{+}$离子 | |
| D. | 品红溶液或高锰酸钾溶液均可鉴别CO2和SO2 |
4.在同温、同压下,相同物质的量的氢气和氦气,具有相同的( )
| A. | 原子数 | B. | 质子数 | C. | 体积 | D. | 质量 |
5.下列事实,其中不能用平衡移动原理解释的是( )
| A. | 向0.1mol/L的CH3COOH溶液中加入少量CH3COONa固体,溶液pH增大 | |
| B. | 在密闭容器中充入一定量NO2建立2NO2(g)?N2O4(g)平衡后,增大压强,体系颜色加深 | |
| C. | 向水中投入金属Na,最终溶液呈碱性 | |
| D. | 在滴有酚酞的Na2CO3溶液中,慢慢滴入BaCl2溶液,溶液的红色逐渐褪去 |

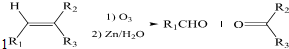

 +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O.
+H2O. .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).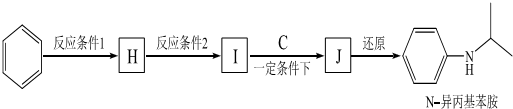
 .
.