题目内容
在25℃时,将两个铜电极插入一定量的硫酸钠饱和溶液中进行电解,通电一段时间后,阴极逸出a mol气体,同时有w g Na2SO4?10H2O晶体析出,若温度不变,剩余溶液中溶质质量分数是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:溶液中溶质的质量分数及相关计算
专题:
分析:电解发生反应:Cu+2H2O
Cu(OH)2↓+H2↑,原硫酸钠溶液为饱和溶液,电解后剩余溶液也为饱和溶液,因此电解析出的晶体和电解消耗的水构成的溶液仍为饱和溶液,三者的质量分数相等.阴极生成气体为氢气,根据Cu+2H2O
Cu(OH)2↓+H2↑可知发生电解的水为2a mol,根据化学式计算晶体中含有Na2SO4的质量,根据质量分数=
×100%计算.
| ||
| ||
| m(溶质) |
| m(溶液) |
解答:
解:电解发生反应:Cu+2H2O
Cu(OH)2↓+H2↑,原硫酸钠溶液为饱和溶液,因此电解析出的晶体和电解消耗的水构成的溶液仍为饱和溶液,三者的质量分数相等,
阴极生成的气体为氢气,根据Cu+2H2O
Cu(OH)2↓+H2↑,可知电解消耗的水为2a mol,故剩余溶液中溶质的质量分数为
×100%=
×100%,
故选D.
| ||
阴极生成的气体为氢气,根据Cu+2H2O
| ||
wg×
| ||
| wg+2amol×18g/mol |
| 71w |
| 161(w+36a) |
故选D.
点评:本题以电解原理为载体,考查溶液质量分数的计算,判断电解析出的晶体和消耗的水构成的溶液仍为饱和溶液是解题的关键,难度中等.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
a mL三种气态烃的混合物和足量的氧气混合点燃爆炸后,恢复到原来的状态(常温常压),气体体积共缩小2a mL(不考虑二氧化碳的溶解).则三种烃可能的组合是( )
| A、相同条件下CH4、C2H4、C3H4任意体积比 |
| B、CH4、C3H6、C2H2保持C3H6:C2H2=1:2(物质的量之比) |
| C、C2H6、C4H6、C2H2同条件下体积比为2:1:1 |
| D、C3H8、C4H8、C2H2质量比为11:14:26 |
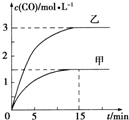 T℃下发生反应:C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、乙两个恒容密闭容器中加入一定量C和H2O,各容器的容积、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示:下列说法正确的是( )
T℃下发生反应:C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、乙两个恒容密闭容器中加入一定量C和H2O,各容器的容积、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示:下列说法正确的是( )| 容器 | 甲 | 乙 |
| 容积 | 0.5L | V |
| 2molC 1molH2O | 4molC 2molH2O |
| A、甲容器中前15min反应的平均速率υ(H2)=0.2 mol?L-1?min-1 |
| B、乙容器的容积V=0.5 L |
| C、向甲容器加入少量C(s),平衡正向移动 |
| D、反应温度升高,平衡常数增大 |
门捷列夫在绘制元素周期表时许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素(与硅处于同族),后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确.根据元素周期律,下列有关X性质的描述中错误的是( )
| A、X单质不易与水反应 |
| B、XO2可被碳还原为X |
| C、XH4的稳定性比SiH4的高 |
| D、X的半径比Si的大 |
在相同条件下,下列气态氢化物的稳定性排列顺序正确的是( )
| A、HF>HCl>HBr>HI |
| B、HCl>HBr>HI>HF |
| C、HBr>HI>HF>HCl |
| D、HI>HBr>HCl>HF |
下列化学用语表达正确的是( )
| A、乙酸的结构简式:C2H4O2 |
B、氢氧化钠的电子式: |
C、Cl离子的结构示意图: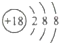 |
| D、NaClO的电离方程式:NaClO=Na++Cl-+O2- |
化学与生活密切相关,下列有关说法正确的是( )
| A、糖类、油脂、蛋白质属于天然高分子化合物 |
| B、维生素C具有还原性,在人体内起抗氧化作用 |
| C、煤经气化和液化两个物理变化过程,可变为清洁能源 |
| D、制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
下列有关溶液组成的描述合理的是( )
| A、在Fe2(SO4)3溶液中可以大量存在:K+、Fe2+、Cl-、Br-、SCN- | ||
| B、c(H+)=1×10-13mol/L的溶液中可以大量存在:Mg2+、Cu2+、HCO3-、NO3- | ||
C、加水稀释时
| ||
| D、在碱性溶液中可以大量存在:S2O32-、AlO2-、SiO32-、S2-、Na+ |
某元素原子最外层只有1个电子,它跟卤素相结合时,所形成的化学键是( )
| A、一定形成共价键 |
| B、一定形成离子键 |
| C、可能形成共价键,也可能形成离子键 |
| D、以上说法都不对 |