题目内容
2.下列关于漂白粉的叙述正确的是( )| A. | 有效成分是CaCl2 | B. | 空气中久置会变质 | ||
| C. | 工业上常用Cl2和消石灰反应制得 | D. | 使用时加浓盐酸可提高漂白效果 |
分析 氯气与石灰乳发生氧化还原反应可制备漂白粉,主要成分为氯化钙、次氯酸钙,有效成分为次氯酸钙,在空气中久置时次氯酸钙与水、二氧化碳反应生成碳酸钙、HClO,HClO光照分解而变质,以此来解答.
解答 解:A.漂白粉的有效成分为Ca(ClO)2,故A错误;
B.次氯酸钙能与空气中的二氧化碳、水反应,发生Ca(ClO)2+H2O+CO2═2HClO+CaCO3↓、2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,从而变质,故B正确;
C.氯气与消石灰反应生成CaCl2、Ca(ClO)2、H2O,反应的方程式为:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,故C正确;
D.使用时加浓盐酸,发生Cl-+ClO-+2H+=H2O+Cl2↑,生成有毒气体,易中毒,故D错误;
故选BC.
点评 本题考查漂白粉的性质及应用,为高频考点,把握漂白粉的制备、漂白原理、使用为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.

练习册系列答案
相关题目
8.下列表达方式正确的是( )
| A. | 24Cr的外围电子排布式:3d44s2 | B. | CO2的立体结构模型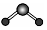 | ||
| C. | 基态碳原子的价电子排布图为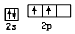 | D. | S2-的结构示意图: |
13.以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀.根据上述实验事实,下列说法中,不正确的是( )
| A. | 溶解度 MnS<PbS | |
| B. | MnS存在沉淀溶解平衡 MnS(s)?Mn2+(aq)+S2-(aq) | |
| C. | Cu2+转化为沉淀的原理为 MnS(s)+Cu2+(aq)═CuS(s)+Mn2+(aq) | |
| D. | 沉淀转化能用于除去溶液中的某些杂质离子 |
10.下列有机化学方程式书写错误的是( )
| A. | CH2═CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl | |
| B. | 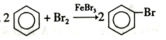 | |
| C. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O |
17.2016杭州G20峰会期间,夜晚的空中被激光照射出美丽的光束,产生此现象主要是因为大气中存在( )
| A. | 纯净物 | B. | 溶液 | C. | 胶体 | D. | 浊液 |
7.下列反应的离子方程式正确的是( )
| A. | 铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 过氧化钠与水反应:Na2O2+H2O=2Na++2OH-+O2↑ | |
| C. | 氯气与水反应:Cl2+H2O=2H++Cl-+ClO- | |
| D. | 碳酸钙与稀盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
14.下列说法中,正确的是( )
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 鸡蛋清遇醋酸铅后产生的沉淀能重新溶于水 | |
| C. | 麦芽糖水解生成互为同分异构体的葡萄糖和果糖 | |
| D. | α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽,只生成2种二肽 |
11.下列解释事实的化学用语正确的是( )
| A. | CO2的水溶液显酸性:CO2+H2O?H2CO3?2H++CO32- | |
| B. | Na2S2O3溶液与稀H2SO4混合产生黄色浑浊:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O | |
| C. | 氢氧化亚铁能与次氯酸反应:Fe(OH)2+2H++2ClO-=Fe2++2H2O+2Cl- | |
| D. | 草酸是二元弱酸,能使酸性高锰酸钾溶液褪色:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O |
12.下列气体中,既有颜色又有毒性的是( )
| A. | N2 | B. | CO | C. | NO2 | D. | NH3 |