题目内容
在稀硫酸中,KMnO4和H2O2能发生氧化还原反应:氧化反应:H2O2-2e-=2H++O2↑ 还原反应:MnO4-+5e-+8H+=Mn2++4H2O
(1)写出该氧化还原反应的离子方程式: .
(2)反应中氧化剂是 ;氧化产物是 ;若有0.5molH2O2参加此反应,电子转移个数为 .
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为 ;这时若有0.5molH2O2发生分解,电子转移个数为 .
(1)写出该氧化还原反应的离子方程式:
(2)反应中氧化剂是
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:(1)依据氧化反应和还原反应电子守恒,合并书写离子方程式;
(2)根据元素化合价变化判断氧化剂,元素化合价降低的物质做氧化剂,元素化合价升高做还原剂被氧化,依据离子方程式计算电子转移数;
(3)锰离子催化过氧化氢分解生成水和氧气,依据分解反应计算电子转移数.
(2)根据元素化合价变化判断氧化剂,元素化合价降低的物质做氧化剂,元素化合价升高做还原剂被氧化,依据离子方程式计算电子转移数;
(3)锰离子催化过氧化氢分解生成水和氧气,依据分解反应计算电子转移数.
解答:
解:(1)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应:
①氧化反应:H2O2-2e-═2H++O2↑
②还原反应:MnO4-+5e-+8H+═Mn2++4H2O
①×5+②×2得到:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O;
故答案为:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O;
(2)反应中化合价降低的元素是锰元素,从+7价降到+2价,所以氧化剂是KMnO4,过氧化氢中氧元素化合价从-1价升高到0价,做还原剂被氧化,为氧化产物,
若有0.5mol H2O2参加此反应,根据离子方程式5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O;可知转移电子数1mol,转移电子个数为6.02×1023,
故答案为:KMnO4;O2;6.02×1023;
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为:2H2O2
2H2O+O2↑; H2O2发生分解,氧元素化合价从-1价变化为0价和-2价,每2mol过氧化氢反应转移电子为2mol,若有0.5mol H2O2发生分解,则转移电子个数为0.5mol,即转移电子个数为3.01×1023;
故答案为:2H2O2
2H2O+O2↑; 3.01×1023.
①氧化反应:H2O2-2e-═2H++O2↑
②还原反应:MnO4-+5e-+8H+═Mn2++4H2O
①×5+②×2得到:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O;
故答案为:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O;
(2)反应中化合价降低的元素是锰元素,从+7价降到+2价,所以氧化剂是KMnO4,过氧化氢中氧元素化合价从-1价升高到0价,做还原剂被氧化,为氧化产物,
若有0.5mol H2O2参加此反应,根据离子方程式5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O;可知转移电子数1mol,转移电子个数为6.02×1023,
故答案为:KMnO4;O2;6.02×1023;
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为:2H2O2
| ||
故答案为:2H2O2
| ||
点评:本题考查氧化还原反应,侧重氧化还原反应基本概念及计算的考查,注重学生知识迁移应用能力的训练,题目难度中等.

练习册系列答案
相关题目
下列各实验装置图与操作正确且能达到实验目的( )
A、 实验室干燥氯气 |
B、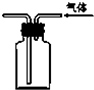 实验室收集SO2气体 |
C、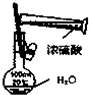 稀释浓硫酸 |
D、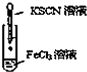 鉴定Fe3+ |
一定条件下,在四个恒定密闭容器中分别进行下列反应,其中依据“容器内气体压强不变”可判定该反应达到平衡状态的是( )
| A、CO2(g)+H2(g)?CO(g)+H2O(g) |
| B、C(s)+CO2(g)?2CO(g) |
| C、2HI(g)?H2(g)+I2(g) |
| D、FeO(s)+CO(g)?Fe(s)+CO2(g) |