题目内容
14.将2aL Al2(SO4)3和(NH4)2SO4的混合物溶液分为两等份,其中一份加入b mol BaCl2,恰好使溶液中的SO42-离子完全沉淀;另一份加入足量强碱并加热可得到c mol NH3气,则原混合溶液中的Al3+离子浓度(mol/L)为( )| A. | $\frac{2b-c}{a}$ | B. | $\frac{2b-c}{2a}$ | C. | $\frac{2b-c}{3a}$ | D. | $\frac{2b-c}{6}$ |
分析 根据SO42-+Ba2+═BaSO4↓计算溶液中的SO42-离子的物质的量,根据NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O计算NH4+的物质的量,再根据c=$\frac{n}{V}$计算SO42-离子、NH4+离子浓度,再利用电荷守恒有3n(Al3+)+c(NH4+)=2c(SO42-),据此计算原溶液中的Al3+浓度.
解答 解:将Al2(SO4)3和(NH4)2SO4的混合溶液2a L分为两等份,每份的体积为a,
向aL混合溶液中加入bmolBaCl2,恰好使溶液中的SO42-离子完全沉淀,则:
SO42-+Ba2+═BaSO4↓
bmol bmol
c(SO42-)=$\frac{bmol}{aL}$=$\frac{b}{a}$mol/L,
向aL混合溶液中加入足量强碱并加热可得到cmolNH3,则:
NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O
cmol cmol
c(NH4+)=$\frac{cmol}{aL}$=$\frac{c}{a}$mol/L,
又溶液不显电性,设原溶液中的Al3+浓度为x,由电荷守恒可知,
x×3+$\frac{c}{a}$mol/L×1=$\frac{b}{a}$mol/L×2,
解得x=$\frac{2b-c}{3a}$mol/L,
故选C.
点评 本题考查混合物的有关计算、物质的量浓度的计算等,题目难度中等,明确发生的离子反应及溶液不显电性是解答本题的关键,注意熟悉物质的量浓度的计算公式.

练习册系列答案
相关题目
4.表为周期表短周期的一部分.下列有关A、B、C、D、E五种元素的叙述,正确的是( )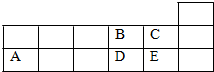

| A. | 它们的简单离子半径大小关系为:A>D>E>B>C | |
| B. | 氧化物的水化物的酸性强弱关系:E>D>A | |
| C. | 化合物E2B的分子中B原子的杂化方式为sp3 | |
| D. | 工业上将E单质通入澄清石灰水中反应制漂白粉 |
5.下列说法正确的是( )
| A. | 1mol任何物质都约含有6.02×1023个原子 | |
| B. | 物质的量为2mol的BaCl2中,含有Cl-个数为2NA | |
| C. | O2的摩尔质量是32 | |
| D. | 摩尔是物质的量的单位 |
2.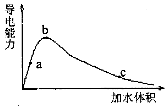 一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
 一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )| A. | 醋酸的电离度:c<b<a | |
| B. | 溶液的PH值:b<a<c | |
| C. | 蘸取a点溶液滴在湿润的PH试纸上,测得PH值一定偏大 | |
| D. | 若分别取a、b、c三点的溶液各10mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a=b=c |
6.下列有关说法不正确的是( )
| A. | BaSO4(s)+4C(s)═BaS(s)+4CO(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 | |
| C. | 己知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ•mol-1,则水电离的热化学方程式为:H2O(l)?H+ (aq)+OH-(aq)△H=+57.3 kJ•mol-1 | |
| D. | 向0.1mol/L的CH3COONa溶液中加入少量醋酸钠固体,c(CH3COO-)/c(Na+ )变大 |
3.下列说法中不正确的是( )
| A. | 三氯蔗糖(C12H19Cl3O8)属于天然的糖类甜味剂 | |
| B. | 未成熟的青苹果肉遇碘酒变蓝色,成熟苹果的汁能发生银镜反应 | |
| C. | 利用盐析的方法可以用来分离、提纯蛋白质 | |
| D. | 酚醛树脂、合成橡胶、有机玻璃都属于有机高分子化合物 |
4.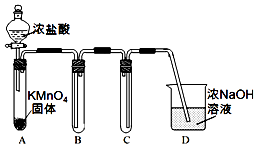 某兴趣小组利用文献资料设计方案对氯及其化合物进行探究.
某兴趣小组利用文献资料设计方案对氯及其化合物进行探究.
I.用高锰酸钾和浓盐酸反应制取氯气
(1)该小组利用如图装置及试剂制备并收集适量Cl2,装置B中收集的气体中所含的杂质有HCl、H2O(g),D的作用是吸收C中逸出的Cl2.
(2)制得的氯气中加入适量水,得到饱和氯水,
饱和氯水中含氯元素的微粒有Cl-、Cl2、ClO-、HClO(写出全部微粒的化学式).
(3)饱和氯水与石灰石的反应是制取较浓HC1O溶液的方法之一.在过量的石灰石中加入饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去,过滤,得到的滤液其漂白性比饱和氯水更强.
①滤液漂白性增强的原因是氯水中存在平衡Cl2+H2O?H++Cl-+HClO,CaCO3与盐酸反应,平衡正向移动,增大了HClO的浓度,漂白效果增强(用化学平衡移动原理解释).
②已知H2CO3的第二电离常数K2=5.6×10-11,HClO的电离常数K=3.0×10-8,写出Cl2与Na2CO3溶液按物质的量之比1:1恰好反应的离子方程式Cl2+H2O+CO32-=HCO3-+HClO+Cl-.
Ⅱ.ClO3-、Cl-和H+反应的探究
(4)KClO3、KCl与硫酸可以反应.该小组设计了系列实验研究反应条件对反应的影响,实验记录如表(实验在室温下进行):
①该系列实验的目的其他条件相同,氢离子或者硫酸浓度不同对化学反应速率的影响.
②烧杯2加水的体积V4应为6 mL,烧杯4中的现象溶液呈黄绿色,生成黄绿色气体.
(5)该小组同学查资料得知:将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量ClO2生成;ClO2沸点为10℃,熔点为-59℃,液体为红色;Cl2沸点为-34℃,液态为黄绿色.设计最简单的实验验证Cl2中含有ClO2收集一试管气体,盖上胶塞,放入冰水混合物中,观察液体(或气体)颜色变化.
 某兴趣小组利用文献资料设计方案对氯及其化合物进行探究.
某兴趣小组利用文献资料设计方案对氯及其化合物进行探究.I.用高锰酸钾和浓盐酸反应制取氯气
(1)该小组利用如图装置及试剂制备并收集适量Cl2,装置B中收集的气体中所含的杂质有HCl、H2O(g),D的作用是吸收C中逸出的Cl2.
(2)制得的氯气中加入适量水,得到饱和氯水,
饱和氯水中含氯元素的微粒有Cl-、Cl2、ClO-、HClO(写出全部微粒的化学式).
(3)饱和氯水与石灰石的反应是制取较浓HC1O溶液的方法之一.在过量的石灰石中加入饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去,过滤,得到的滤液其漂白性比饱和氯水更强.
①滤液漂白性增强的原因是氯水中存在平衡Cl2+H2O?H++Cl-+HClO,CaCO3与盐酸反应,平衡正向移动,增大了HClO的浓度,漂白效果增强(用化学平衡移动原理解释).
②已知H2CO3的第二电离常数K2=5.6×10-11,HClO的电离常数K=3.0×10-8,写出Cl2与Na2CO3溶液按物质的量之比1:1恰好反应的离子方程式Cl2+H2O+CO32-=HCO3-+HClO+Cl-.
Ⅱ.ClO3-、Cl-和H+反应的探究
(4)KClO3、KCl与硫酸可以反应.该小组设计了系列实验研究反应条件对反应的影响,实验记录如表(实验在室温下进行):
| 烧杯编号 | 1 | 2 | 3 | 4 |
| 氯酸钾饱和溶液 | 1mL | V1mL | V2mL | V3mL |
| 氯化钾固体 | 1g | 1g | 1g | 1g |
| 水 | 8mL | V4mL | 3mL | 0mL |
| 硫酸(6mol/L) | V5mL | 2mL | V6mL | 8mL |
| 现象 | 无现象 | 溶液呈浅黄色 | 溶液呈黄绿色,生成浅黄绿色气体 |
②烧杯2加水的体积V4应为6 mL,烧杯4中的现象溶液呈黄绿色,生成黄绿色气体.
(5)该小组同学查资料得知:将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量ClO2生成;ClO2沸点为10℃,熔点为-59℃,液体为红色;Cl2沸点为-34℃,液态为黄绿色.设计最简单的实验验证Cl2中含有ClO2收集一试管气体,盖上胶塞,放入冰水混合物中,观察液体(或气体)颜色变化.
