题目内容
4.某有机物分子中有 n 个CH 2,m 个 ,a个CH 3,其余为OH,则该物质分子中OH的个数可能为( )
,a个CH 3,其余为OH,则该物质分子中OH的个数可能为( )| A. | m-a | B. | n+m+a | C. | m+1-a | D. | m+2-a |
分析 该有机物中含有a个-CH3,n 个-CH2-,m个 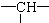 ,其余为OH,说明该物质属于饱和醇,将OH原子换为H原子就是烷烃结构,根据烷烃通式计算出H原子个数,计算已知的H原子个数,剩余的就是OH原子个数,据此分析解答.
,其余为OH,说明该物质属于饱和醇,将OH原子换为H原子就是烷烃结构,根据烷烃通式计算出H原子个数,计算已知的H原子个数,剩余的就是OH原子个数,据此分析解答.
解答 解:某有机物链状分子中含有a个-CH3,n 个-CH2-,m个 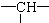 ,其余为OH,说明该物质属于饱和醇,将OH原子换为H原子就是烷烃结构,该分子中C原子个数=(a+n+m),根据烷烃通式知H原子个数=2(a+n+m)+2,a个-CH3,n 个-CH2-,m个
,其余为OH,说明该物质属于饱和醇,将OH原子换为H原子就是烷烃结构,该分子中C原子个数=(a+n+m),根据烷烃通式知H原子个数=2(a+n+m)+2,a个-CH3,n 个-CH2-,m个 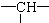 中H原子总数=3a+2n+m,则缺少的H原子个数=2(a+n+m)+2-(3a+2n+m)=m+2-a,所以OH个数为m+2-a;
中H原子总数=3a+2n+m,则缺少的H原子个数=2(a+n+m)+2-(3a+2n+m)=m+2-a,所以OH个数为m+2-a;
故选D.
点评 本题考查常见有机物结构,侧重考查学生知识迁移能力,采用补缺法分析解答即可,题目难度不大.

练习册系列答案
相关题目
4.在含有稀硫酸的硫酸铁溶液中,下列离子能大量共存的是( )
| A. | HCO3- | B. | NO3- | C. | SCN- | D. | Ba2+ |
15.将适量铁粉放入Fe2(SO4)3溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等.则已经反应的Fe3+和未反应的Fe3+物质的量之比为( )
| A. | 2:3 | B. | 3:2 | C. | 1:2 | D. | 2:1 |
12.下表为元素周期表的短周期部分.
请参照元素a-h在表中的位置,根据判断出的元素回答问题:
(1)h原子核外有4 种不同伸展方向的电子云,最外层共有7 种不同运动状态的电子.
(2)比较d、e元素常见离子的半径大小(用化学式表示)O2->Na+;b、c 两元素非金属性较强的是(写元素符号)N,写出证明这一结论的一个化学方程式2HNO3+Na2CO3 =2NaNO3+CO2↑+H2O.
(3)d、e元素形成的四原子化合物的电子式为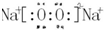 ;b、g元素形成的分子bg2为非极性分子(填写“极性”或“非极性”).
;b、g元素形成的分子bg2为非极性分子(填写“极性”或“非极性”).
上述元素可组成盐R:ca4f(gd4)2,和盐S:ca4agd4,
(4)相同条件下,0.1mol/L 盐R中c(ca4+)小于(填“等于”、“大于”或“小于”)0.1mol/L 盐S中c(ca4+).
(5)向盛有10mL1mol/L盐S溶液的烧杯中滴加1mol/L NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
(6)向盛有10mL 1mol/L盐 R溶液的烧杯中滴加1mol/L NaOH溶液32mL后,继续滴加至35mL写出此时段(32mL-35mL)间发生的离子方程式:NH4++OH-=NH3•H2O.若在10mL 1mol/L 盐R溶液的烧杯中加20mL1.2mol/L Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为0.022mol.
| a | |||||||
| b | c | d | |||||
| e | f | g | h |
(1)h原子核外有4 种不同伸展方向的电子云,最外层共有7 种不同运动状态的电子.
(2)比较d、e元素常见离子的半径大小(用化学式表示)O2->Na+;b、c 两元素非金属性较强的是(写元素符号)N,写出证明这一结论的一个化学方程式2HNO3+Na2CO3 =2NaNO3+CO2↑+H2O.
(3)d、e元素形成的四原子化合物的电子式为
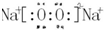 ;b、g元素形成的分子bg2为非极性分子(填写“极性”或“非极性”).
;b、g元素形成的分子bg2为非极性分子(填写“极性”或“非极性”).上述元素可组成盐R:ca4f(gd4)2,和盐S:ca4agd4,
(4)相同条件下,0.1mol/L 盐R中c(ca4+)小于(填“等于”、“大于”或“小于”)0.1mol/L 盐S中c(ca4+).
(5)向盛有10mL1mol/L盐S溶液的烧杯中滴加1mol/L NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
(6)向盛有10mL 1mol/L盐 R溶液的烧杯中滴加1mol/L NaOH溶液32mL后,继续滴加至35mL写出此时段(32mL-35mL)间发生的离子方程式:NH4++OH-=NH3•H2O.若在10mL 1mol/L 盐R溶液的烧杯中加20mL1.2mol/L Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为0.022mol.
19.下列反应的离子方程式书写正确的是( )
| A. | 铁粉加入三氯化铁溶液中:Fe+Fe3+═Fe2+ | |
| B. | 金属铝溶于氢氧化钠溶液 Al+2OH-═AlO2-+H2↑ | |
| C. | 金属铝溶于盐酸中:Al+6H+═Al3++3H2↑ | |
| D. | FeCl2溶液中加入氯水:Cl2+2 Fe2+═2 Fe3++2Cl- |
9.离子方程式Ca2++2HCO3-+2OH-→CaCO3↓+CO32-+2H2O不能表示( )
| A. | Ca(HCO3)2溶液与NaOH溶液反应 | B. | NaHCO3溶液与澄清石灰水反应 | ||
| C. | KHCO3溶液与澄清石灰水反应 | D. | Ca(HCO3)2溶液与澄清石灰水反应 |
13.下列物质不能通过化合反应或置换反应生成的是( )
| A. | Al2O3 | B. | HF | C. | Fe3O4 | D. | HClO |
14.对于胃溃疡较重的病人可使用的抑酸剂是( )
| A. | CaO | B. | Al(OH)3 | C. | NaHCO3 | D. | MgCO3 |
 .
.