题目内容
2.在某一化学反应A+3B═2C+D中,反应物A的浓度在20s内由1.0mol/L变成0.2mol/L,则在这20s内用C表示的平均反应速率为( )| A. | v(C)=0.01 mol/(L•s) | B. | v(C)=0.8 mol/(L•s) | C. | v(C)=0.04 mol/(L•s) | D. | v(C)=0.08 mol/(L•s) |
分析 根据化学反应速率的定义和化学反应速率之比等化学计量数之比进行计算.
解答 解:v(A)=(1.0-0.2)÷20=0.04mol/(L•s),v(C):v(A)=2:1,故v(C)=2v(A)=2×0.04mol/(L•s)=0.08mol/(L•s),
故选D.
点评 本题考查化学反应速率的相关计算,把握化学反应速率的定义和化学反应速率之比等化学计量数之比为解答的关键,难度不大.

练习册系列答案
相关题目
7.下列各组顺序排列不正确的是( )
| A. | 熔点:SiO2>NaCl>CO2 | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 金属性:Na<Mg<Al | D. | 酸性强弱:H2SiO3<H2CO3<HNO3 |
11.下列有关氯离子电子式表述正确的是( )
| A. | 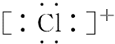 | B. | 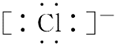 | C. | 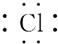 | D. | 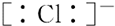 |
 ;
;
 .
.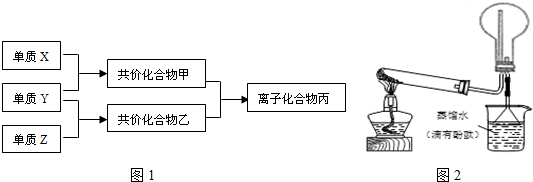
 ;甲的电子式:
;甲的电子式: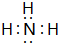 ;
;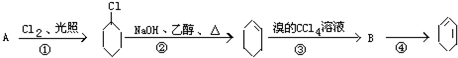
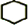 ,B的结构简式是
,B的结构简式是 .
. +2NaBr+2H2O.
+2NaBr+2H2O.