题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
①1L 2mol?L-1MgCl2溶液中所含Cl-数为4NA
②69g NO2、N2O4中所含的N原子数为1.5NA
③1mol?L-1 K2SO4溶液中阴阳离子的总数为1.5NA
④27g Al3+的核外电子数为10NA
⑤在标准状况下,22.4L CCl4中所含CCl4分子数为NA.
①1L 2mol?L-1MgCl2溶液中所含Cl-数为4NA
②69g NO2、N2O4中所含的N原子数为1.5NA
③1mol?L-1 K2SO4溶液中阴阳离子的总数为1.5NA
④27g Al3+的核外电子数为10NA
⑤在标准状况下,22.4L CCl4中所含CCl4分子数为NA.
| A、①③⑤ | B、②④⑤ |
| C、①②④ | D、①③④ |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:①根据公式n=cv,N=nNA计算;
②按NO2、N2O4中N与O个数比为1:2,按照69gNO2计算即可;
③缺少溶液的体积,不能计算;
④根据n=
计算Al3+的物质的量,根据N=nNA计算离子数,每个 Al3+含有10个电子;
⑤标准状况下,CCl4不是气体.
②按NO2、N2O4中N与O个数比为1:2,按照69gNO2计算即可;
③缺少溶液的体积,不能计算;
④根据n=
| n |
| M |
⑤标准状况下,CCl4不是气体.
解答:
解:①氯化镁的物质的量为1L×2mol?L-1=2mol,溶液中含有4mol氯离子,数目为4NA,故①正确;
②69gNO2的物质的量为
=1.5mol,分子数为1.5NA,因此N原子数为1.5NA,故②正确;
③缺少溶液的体积,不能计算,故③错误;
④n( Al3+)=
=1mol,Al3+数为NA,每个 Al3+含有10个电子,因此电子数为10NA,故④正确;
⑤标准状况下,CCl4不是气体,不能带入n=
计算,故⑤错误;
故选C.
②69gNO2的物质的量为
| 69g |
| 46g/nol |
③缺少溶液的体积,不能计算,故③错误;
④n( Al3+)=
| 27g |
| 27g/mol |
⑤标准状况下,CCl4不是气体,不能带入n=
| V |
| Vm |
故选C.
点评:本题借助阿伏伽德罗常数,考查了以物质的量为中心的计算,应用气体摩尔体积时,一定要看清物质状态.

练习册系列答案
相关题目
只用胶头滴管和试管,不用其它任何试剂,就可以区别的下列溶液是( )(浓度均为0.1mol/L)
①氯化钙和碳酸钠 ②碳酸钠和硫酸 ③氢氧化钙和碳酸氢钠 ④偏铝酸钠和盐酸.
①氯化钙和碳酸钠 ②碳酸钠和硫酸 ③氢氧化钙和碳酸氢钠 ④偏铝酸钠和盐酸.
| A、②③④ | B、②④ |
| C、①②③④ | D、①③ |
下列物质中,能导电且为电解质的是( )
| A、熔融态的NaC1 | B、固体NaOH |
| C、铁 | D、稀硫酸 |
下列各组内两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A、氢氧化钠与硝酸;氢氧化钾与盐酸 |
| B、碳酸钠与硝酸;碳酸氢钠与盐酸 |
| C、硫酸与氢氧化钡;硫酸雨氯化钡 |
| D、硫酸铜与氢氧化钡;氯化铜与氢氧化钡 |
分析下列各物质的物理性质,可判断其固态不属于分子晶体的是( )
| A、碳化铝,黄色晶体,熔点2200℃.熔融态不导电 |
| B、溴化铝,无色晶体,熔点98℃,熔融态不导电 |
| C、五氟化钒,无色晶体,熔点19.5℃,易溶于乙醇、氯仿、丙铜中 |
| D、干冰,无色晶体,熔融时不导电 |

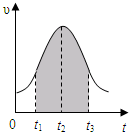 实验测得0.01mol/L的KMnO4的硫酸溶液和0.1mol/L的H2C2O4溶液等体积混合后,反应速率υ[mol/(L?s)]与反应时间t(s)的关系如图所示.该反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
实验测得0.01mol/L的KMnO4的硫酸溶液和0.1mol/L的H2C2O4溶液等体积混合后,反应速率υ[mol/(L?s)]与反应时间t(s)的关系如图所示.该反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O