题目内容
根据你已有的知识和经验,分析下列过程的焓变、熵变,并判断反应的方向.
(1)H+(aq)+OH-(aq)=H2O (l)△S=+80.7J?mol-1?K-1,△H 0,△S 0,该反应 (自发或非自发)
(2)TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g)△H=+161.9kJ?mol-1△S=-38.4J?mol-1?K-1该反应 (自发或非自发)
(1)H+(aq)+OH-(aq)=H2O (l)△S=+80.7J?mol-1?K-1,△H
(2)TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g)△H=+161.9kJ?mol-1△S=-38.4J?mol-1?K-1该反应
考点:焓变和熵变
专题:化学反应中的能量变化
分析:反应能否自发进行的判据为:△H-T△S,只有△H-T△S<0的反应才能自发进行,据此解答.
解答:
解:(1)酸碱中和反应为放热反应,所以△H<0,△S为正值所以△S>0,则△H-T△S一定小于0,所以该反应能自发进行;
故答案为:<;>;自发;
(2)TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g)△H=+161.9kJ?mol-1△S=-38.4J?mol-1?K-1该反应△H>0,△S<0,则:△H-T△S一定大于0,所以反应不能自发进行;
故答案为:非自发.
故答案为:<;>;自发;
(2)TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g)△H=+161.9kJ?mol-1△S=-38.4J?mol-1?K-1该反应△H>0,△S<0,则:△H-T△S一定大于0,所以反应不能自发进行;
故答案为:非自发.
点评:本题考查了反应焓变、熵变与反应能否自发进行的关系,明确反应能否自发进行的判断依据是解题关键,注意单位统一.

练习册系列答案
相关题目
下列装置中四块相同的Zn片,放置一段时间后腐蚀速率由慢到快的顺序是( )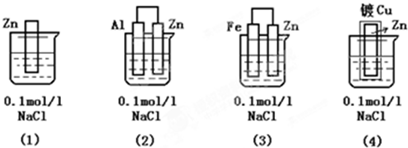

| A、①②③④ | B、④②①③ |
| C、③①②④ | D、②①③④ |
温家宝总理在2010年政府工作报告中提出,推广高效节能技术,提倡低碳生活,积极发展新能源和可再生能源.下列有关做法与此不相符的是( )
| A、大力开发丰富的煤炭资源,减少对石油的依赖 |
| B、在西部和沿海地区兴建风力发电站,解决能源问题 |
| C、世博会很多场馆的外壳使用非晶硅薄膜,以充分利用太阳能,体现低碳经济 |
| D、世博停车场安装催化光解设施,可将汽车尾气中CO和NOx反应生成无毒气体 |

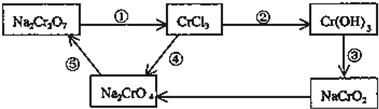
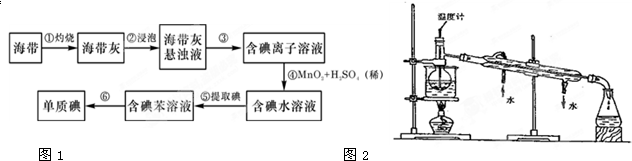
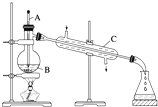 选择下列实验方法分离物质,将分离方法的序号填在横线上.
选择下列实验方法分离物质,将分离方法的序号填在横线上.