题目内容
10.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成: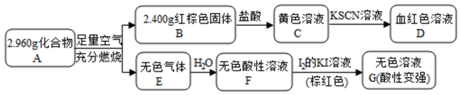
请回答:
(1)A的化学式为Fe3S4.A煅烧生成B和E的化学方程式为4Fe3S4+25O2$\frac{\underline{\;高温\;}}{\;}$6Fe2O3+16SO2.
(2)溶液C可溶解铜片,反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,例举该反应的一个实际应用是刻饰铜线路板.
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518g/L),该气体分子的电子式为
 . 该反应的离子方程式为Fe3S4+6H+=3Fe2++S+3H2S↑.
. 该反应的离子方程式为Fe3S4+6H+=3Fe2++S+3H2S↑.
分析 C加入KSCN,D为血红色溶液,可知C为FeCl3,D为Fe(SCN)3等,可知B为Fe2O3,且n(Fe2O3)=$\frac{2.400g}{160g/mol}$=0.015mol,n(Fe)=0.03mol,m(Fe)=0.03mol×56g/mol=1.68g,A燃烧生成的无色气体E溶液水得到酸性溶液,加入碘的KI溶液,得到无色溶液,说明碘可氧化E的水溶液,E应为SO2,F为H2SO3,G含有和H2SO4和HI,可知A含有Fe、S元素,且m(S)=2.96g-1.68g=1.28g,n(S)=$\frac{1.28g}{32g/mol}$=0.04mol,可知n(Fe):n(S)=3:4,应为Fe3S4,以此解答该题
解答 解:(1)由以上分析可知,A为Fe3S4,B为Fe2O3,E应为SO2,则A煅烧生成B和E的化学方程式为4Fe3S4+25O2$\frac{\underline{\;高温\;}}{\;}$6Fe2O3+16SO2,
故答案为:Fe3S4;4Fe3S4+25O2$\frac{\underline{\;高温\;}}{\;}$6Fe2O3+16SO2;
(2)由以上分析可知,溶液C为FeCl3,可氧化铜,常用于刻饰铜线路板,反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;刻饰铜线路板;
(3)化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518g•L-1),淡黄色不溶物为S,气体的相对分子质量为1.518×22.4L=34,为H2S气体,电子式为 ,反应的离子方程式为Fe3S4+6H+=3Fe2++S+3H2S↑,
,反应的离子方程式为Fe3S4+6H+=3Fe2++S+3H2S↑,
故答案为: ;Fe3S4+6H+=3Fe2++S+3H2S↑.
;Fe3S4+6H+=3Fe2++S+3H2S↑.
点评 本题综合考查无机物的推断,为高考常见题型,侧重于学生的分析、计算和实验能力的考查,注意把握物质的性质以及反应现象,结合质量守恒推断物质的组成,难度中等.

 阶梯计算系列答案
阶梯计算系列答案| A. | Al2(SO4)3═2Al3++3SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | H2O═O2-+2H+ | D. | Na2CO3═Na2++CO32- |
 碳氧化物研究
碳氧化物研究(1)在体积可变 (活塞与容器之间的摩擦力忽略不计)的密闭容器如右图所示,现将3molH2和2molCO放入容器中,移动活塞至体积V为2L,用铆钉固定在A、B点,发生合成甲醇的反应如下:CO(g)+2H2(g)═CH3OH(g),测定不同条件、不同时间段内的CO的转化率,得到如表数据:
| CO的转化率 T(℃) | 10min | 20min | 30min | 40min |
| T1 | 20% | 55% | 65% | 65% |
| T2 | 35% | 50% | a1 | a2 |
②T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人6molCO,此时v(正)< v(逆)(选填“>”、“<”或“=”).
③现有以下几种情况放入该体积可变的密闭容器中,请选出T2℃下达到的平衡状态与①中T2℃下的平衡状态一致的是
A、2mol H2+1molCO+1molCH3OH
B、0.5mol H2+1.5molCH3OH
C、1mol H2+1molCO+1molCH3OH
D、2mol H2+4molCH3OH
(2)一定条件下可用甲醇与CO反应生成醋酸消除CO污染.常温下,将a mol/L的醋酸与b mol/L Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=$\frac{2b}{a-2b}$×10-7L/mol(用含a和b的代数式表示).
| A. | 第二个反应的平衡常数为1 | |
| B. | 第二个反应的平衡常数为0.05 | |
| C. | 第二个反应达到平衡时,H2的平衡浓度为0.25mol/L | |
| D. | 第二个反应达到平衡时,HI(g)的平衡浓度为0.25 mol/L |
| A. | 原子半径:W>Z>Y>X | |
| B. | 最简单氢化物的稳定性:Y>Z | |
| C. | X和W形成的化合物属于离子化合物 | |
| D. | 由X、Y、Z三种元素组成的化合物一定显酸性 |
| A. | 胶体化学可用于制备纳米材料 | |
| B. | 钛合金主要用于尖端领域 | |
| C. | 压电陶瓷可实现化学能与电能的转化 | |
| D. | 稀土元素大大改善合金性能被称为冶金工业的维生素 |
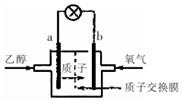 乙醇燃料电池中采用磺酸类质子溶剂,在200℃左右时供电,电池总反应为:
乙醇燃料电池中采用磺酸类质子溶剂,在200℃左右时供电,电池总反应为:C2H5OH+302=2CO2+3H2O,电池示意如图.下列说法中正确的是( )
| A. | 电池工作时.质子向电池的负极迁移 | |
| B. | 电池工作时.电子由b极沿导线流向a极 | |
| C. | a极上发生的电极反应是:C2H5OH+3H2O+12e一=2CO2+12H+ | |
| D. | -b极上发生的电极反应是:4H++O2+4e一=2H2O |
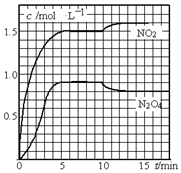 向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应: