题目内容
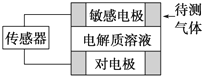
14.气体的自动化检测中常常应用原电池原理的传感器.如图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号.下表列出了待测气体及敏感电极上部分反应产物.则下列说法中正确的是( )| 待测气体 | 敏感电极部分产物 |
| NO2 | NO |
| Cl2 | HCl |
| CO | CO2 |
| H2S | H2SO4 |
| A. | 上述气体检测时,敏感电极均作原电池正极 | |
| B. | 检测Cl2气体时,敏感电极的电极反应为2Cl--2e-═Cl2 | |
| C. | 检测H2S气体时,对电极充入空气,对电极上电极反应式为O2+2H2O+4e-═4OH- | |
| D. | 检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小不相同 |
分析 A.失电子发生氧化反应的电极是负极、得电子发生还原反应的电极是正极;
B.检测氯气时,氯气得电子生成氯离子;
C.检测硫化氢时,硫化氢生成硫酸,硫元素发生氧化反应,则其所在电极为负极;
D.产生的电流大小与失电子多少有关.
解答 解:A.失电子发生氧化反应的电极是负极、得电子发生还原反应的电极是正极,根据待测气体和反应产物可知,部分气体中元素化合价上升,部分气体中元素的化合价下降,所以敏感电极不一定都做电池正极,故A错误;
B.检测氯气时,氯气得电子生成氯离子,电极反应式为Cl2+2e-═2Cl-,故B错误;
C.检测硫化氢时,硫化氢生成硫酸,硫元素化合价由-2价变为+6价而发生氧化反应,则其所在电极为负极,正极上氧气得电子和氢离子反应生成水,电极电极反应式为O2+4H++4e-═2H2O,故C错误;
D.产生的电流大小与失电子多少有关,检测H2S和CO体积分数相同的两份空气样本时,硫化氢失去电子数大于CO,所以产生电流大小不同,故D正确;
故选D.
点评 本题考查了原电池原理,根据元素化合价变化确定正负极,正确判断正负极是解本题关键,难点是电极反应式的书写,注意产生电流与相同物质的量的物质得失电子多少有关,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.原子结构模型的简历和发展与科学实验紧密相关.下列对应关系错误的是( )
| A. | 道尔顿发现原子--“空心球”模型 | |
| B. | 汤姆逊发现电子--“葡萄干布丁”模型 | |
| C. | 卢瑟福进行α粒子散射实验--“核式”模型 | |
| D. | 玻尔解释氢原子光谱--“电子分层排布”模型 |
5.苯丙酸可用作医药中间体,其结构简式如图.与苯丙酸互为同分异构体、含有苯环结构且能与碳酸氢钠溶液反应生成气体的结构有(不考虑立体异构)( )
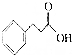

| A. | 13种 | B. | 12种 | C. | 11种 | D. | 10种 |
2.下列有机反应属于加聚反应的是( )
| A. | CH4+Cl2 $\stackrel{光}{→}$ CH3Cl+HCl | B. | nCH2=CH2$\stackrel{催化剂}{→}$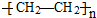 | ||
| C. |  +3H2$→_{△}^{Ni}$ +3H2$→_{△}^{Ni}$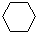 | D. | 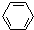 +HNO3$→_{60℃}^{浓H_{2}SO_{4}}$ +HNO3$→_{60℃}^{浓H_{2}SO_{4}}$ +H2O +H2O |
9.已知25℃时部分弱电解质的电离平衡常数数据如表所示:
下列物质的量浓度均为0.1mol•L-1的四种溶液中pH最大的是( )
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
| A. | CH3COONa | B. | Na2CO3 | C. | NaClO | D. | NaHCO3 |
19.下列除去杂质的实验方法正确的是( )
| A. | 除去CO中混有的少量O2:通过灼热的Cu网后收集气体 | |
| B. | 除去SO2中混有的CO2:可通过盛有KMnO4溶液的装置洗气 | |
| C. | 除去FeCl3酸性溶液中少量的FeCl2:加入稍过量双氧水后放置 | |
| D. | 除去SiO2中的Fe2O3:可加入NaOH溶液后过滤 |
6.下列有关苯酚的实验事实中,能说明侧链对苯环性质有影响的是( )
| A. | 1mol苯酚与3mol H2发生加成反应 | B. | 苯酚能和NaOH溶液反应 | ||
| C. | 苯酚燃烧产生带浓烟的火焰 | D. | 苯酚与浓溴水反应生成三溴苯酚 |
3.下列实验叙述正确的是( )
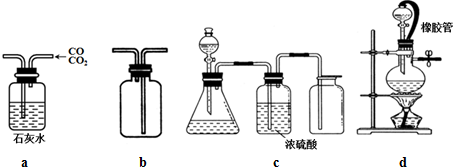

| A. | 用a装置除去混合气体中的杂质CO2 | |
| B. | 用b装置排气法收集H2、NH3、Cl2 | |
| C. | c装置用于碳酸钙和浓盐酸反应制取纯净CO2 | |
| D. | d中橡胶管可使烧瓶内的压强与大气压保持一致,便于液体滴下 |
4.如图装置能达到实验目的是( )
| A. | 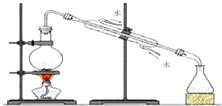 制取少量纯净的水 | B. |  除去Cl2中HCl杂质 | ||
| C. |  烧瓶内形成蓝色喷泉 | D. | 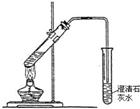 探究NaHCO3的热稳定性 |