题目内容
6.在相同的温度下,已知反应:①N2(g)+O2(g)?2NO(g)的平衡常数K=3.84×10-31;
②2SO2(g)+O2(g)?2SO3(g)的平衡常数K=3.10×1025.
则在该温度下,两个化学反应的反应程度之间的关系为( )
| A. | ①>② | B. | ①<② | C. | ①=② | D. | 不能确定 |
分析 在一定温度下,平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度的幂次方乘积,所以平衡常数在一定条件下反映了反应进行的程度大小,虽然这两个反应平衡常数的表达不一样,但由于它们的数值相关太大,所以据此可以判断反应程度的大小.
解答 解:在一定温度下,平衡常数等于生成物浓度的系数次幂之积除以反应物浓度的系数次幂之积,所以平衡常数在一定条件下反映了反应进行的程度大小,由于反应①的K=3.84×10-31,反应②K=3.10×1025,反应①的K远远小于反应②的K,所以反应①的反应程度小于反应②,
故选B.
点评 本题主要考查了平衡常数的意义,难度不大,虽然这两个反应平衡常数的表达不一样,但由于它们的数值相关太大,所以可以判断出反应进行程度大小,这是解题的难点.

练习册系列答案
相关题目
16.下列说法不正确的是( )
| A. | 将等体积、等物质的量浓度的HA(HA为弱酸)与NaA混合,所得混合液的酸碱性取决于Ka(HA)的大小 | |
| B. | CH3COOH 溶液加水稀释后,溶液中c(H+)/c(CH3COO-) 的值减小 | |
| C. | 某氨水的pH=a,某盐酸的pH=b,已知a+b=14,将上述氨水与盐酸等体积混合后,溶液中各种离子浓度的关系为c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | 等物质的量的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)═c(HCO3-)+c(H2CO3)+c(CO32-) |
17.Ca(OH)2在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是( )
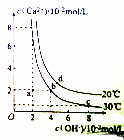

| A. | 20℃时,Ca(OH)2溶解度大于30℃时,Ca(OH)2的溶解度 | |
| B. | 30℃时,Ca(OH)2的饱和溶液中加入少量NaOH固体,Ca(OH)2的Ksp不变 | |
| C. | 30℃时,Ca(OH)2的Ksp等于3.2×10-5 | |
| D. | 20℃时,向Ca(OH)2的饱和溶液中加入少量CaO固体并维持温度不变,溶液的pH增大 |
14.下列物质中,属于电解质的是( )
| A. | 氯化氢 | B. | 石墨 | C. | NaCl溶液 | D. | 蔗糖 |
1.下列叙述正确的是( )
| A. | 1mol任何气体的气体摩尔体积都约为22.4L/mol | |
| B. | 常温常压下,11.2LO3中所含氧原子个数等于1.5NA | |
| C. | 标准状况下,1mol CCl4所占的体积约为22.4L | |
| D. | 同温、同压下,相同体积的一氧化碳和二氧化碳的质量比为7:11 |
18.下列反应中,可用离子方程式H++OH-═H2O表示的是( )
| A. | 氢氧化钡和稀硫酸反应 | B. | 氢氧化铜和稀硝酸反应 | ||
| C. | 稀硫酸和氢氧化钾反应 | D. | 氢氧化钠和盐酸反应 |
15.在0.10mol•L-1 NH3•H2O的溶液中,加水稀释后,引起的变化是( )
| A. | 溶液的pH增大 | B. | NH3•H2O的电离平衡常数增大 | ||
| C. | NH3•H2O的电离程度增大 | D. | NH3•H2O溶液中所有离子浓度减小 |
5. 苯乙烯是重要的基础有机原料.工业中用乙苯(C6 H5-CH2 CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6 H5-CH=CH2)的反应方程式为:
苯乙烯是重要的基础有机原料.工业中用乙苯(C6 H5-CH2 CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6 H5-CH=CH2)的反应方程式为:
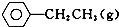 ?催化剂
?催化剂 ═CH2(g)+H2(g)
═CH2(g)+H2(g)
(1)向体积为VL的密闭容器中充入a mol乙苯,反应达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示:由图可知:在600℃时,平衡体系中苯乙烯的物质的量分数为25%,则:
①氢气的物质的量分数为25%;
②乙苯的平衡转化率为33.3%;
③计算此温度下该反应的平衡常数$\frac{a}{6V}$.
(2)已知某温度下,当压强为101.3kPa时,该反应中乙苯的平衡转化率为30%;在相同温度下,若反应体系中加入稀释剂水蒸气并保持体系总压为101.3kPa,则乙苯的平衡转化率>30%(填“>、=、<”).
(3)已知:
计算上述反应的△H=+124kJ/mol.
 苯乙烯是重要的基础有机原料.工业中用乙苯(C6 H5-CH2 CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6 H5-CH=CH2)的反应方程式为:
苯乙烯是重要的基础有机原料.工业中用乙苯(C6 H5-CH2 CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6 H5-CH=CH2)的反应方程式为: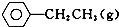 ?催化剂
?催化剂 ═CH2(g)+H2(g)
═CH2(g)+H2(g)(1)向体积为VL的密闭容器中充入a mol乙苯,反应达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示:由图可知:在600℃时,平衡体系中苯乙烯的物质的量分数为25%,则:
①氢气的物质的量分数为25%;
②乙苯的平衡转化率为33.3%;
③计算此温度下该反应的平衡常数$\frac{a}{6V}$.
(2)已知某温度下,当压强为101.3kPa时,该反应中乙苯的平衡转化率为30%;在相同温度下,若反应体系中加入稀释剂水蒸气并保持体系总压为101.3kPa,则乙苯的平衡转化率>30%(填“>、=、<”).
(3)已知:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ/mol | 412 | 348 | 612 | 436 |