题目内容
6.标出电子转移的方向和数目:KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O,该反应的还原剂是HCl,如果有6.72L Cl2(标准状况)生成,则转移电子的个数约为3.01×1023.分析 由KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O可知,KClO3中Cl元素的化合价由+5价降低为0,HCl中Cl元素的化合价由-1价升高为0,根据电子转移和氯气之间的关系进行计算解答.
解答 解:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O的反应中,KClO3中Cl元素的化合价由+5价降低为0,氧化剂是KClO3,被还原,还原产物为Cl2,还原剂是HCl,双线桥法表示氧化还原反应为 ,如果有3mol Cl2(标准状况)生成,则转移电子5mol,如果有6.72L级0.3mol Cl2(标准状况)生成,则转移电子0.5mol,个数是3.01×1023,故答案为:
,如果有3mol Cl2(标准状况)生成,则转移电子5mol,如果有6.72L级0.3mol Cl2(标准状况)生成,则转移电子0.5mol,个数是3.01×1023,故答案为: ;HCl;3.01×1023.
;HCl;3.01×1023.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
相关题目
14.现有三组溶液:①汽油和氯化钠溶液 ②39%的酒精溶液 ③碘的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 分液、蒸馏、萃取 | C. | 萃取、蒸馏、分液 | D. | 蒸馏、萃取、分液 |
11.下列叙述不正确的是( )
| A. | C60能溶于二硫化碳中形成无色透明的溶液,可以用相似相溶原理解释 | |
| B. | 向含有Fe2+的溶液中滴加无色的铁氰化钾溶液,可以观察到蓝色沉淀产生 | |
| C. | 甲烷是空间正四面体结构,四个氢的相对位置完全等效,其任意取代物都不会产生同分异构现象 | |
| D. | 电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述 |
18.具有“-CH2OH”结构的醇类物质中,能被酸性高锰酸钾溶液氧化成相应的酸.分子式为C5Hl2O可被氧化成酸的醇共有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
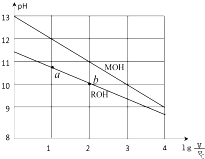 室温下,将浓度均为0.10mol/L体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随$lg\frac{V}{V_0}$的变化如图所示,下列叙述错误的是( )
室温下,将浓度均为0.10mol/L体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随$lg\frac{V}{V_0}$的变化如图所示,下列叙述错误的是( )
 ;
;