题目内容
若某原子的摩尔质量为M g?mol-1,则一个该原子的真实质量是( )
| A、M g | ||
B、
| ||
C、
| ||
D、
|
考点:摩尔质量
专题:阿伏加德罗常数和阿伏加德罗定律
分析:根据1mol任何微粒的数目均为 6.02×10-23个,结合阿伏加德罗常数的含义来计算.
解答:
解:假设有1mol该原子,由摩尔质量知道质量是Mg,1mol原子有阿伏加德罗常数NA个(NA=6.02×1023),
所以NA个原子的质量是Mg,即1个原子的质量是
(NA=6.02×10-23).
故选C.
所以NA个原子的质量是Mg,即1个原子的质量是
| M |
| NA |
故选C.
点评:本题考查了学生阿伏加德罗常数的含义,可以根据所学知识来回答,较简单.

练习册系列答案
相关题目
下列离子方程式不正确的是( )
| A、石英与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
| B、硅与烧碱溶液反应:Si+2OH-+H2O═SiO32-+2H2↑ |
| C、向小苏打溶液中加入过量的石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
| D、往水玻璃中加入盐酸:2H++SiO32-═H2SiO3↓ |
用惰性电极电解下列溶液,一段时间后,阴极质量增加,电解液的pH下降的是( )
①CuSO4 ②BaCl2 ③AgNO3 ④H2SO4.
①CuSO4 ②BaCl2 ③AgNO3 ④H2SO4.
| A、①② | B、②④ | C、①④ | D、①③ |
某学生用0.1000mol?L-1标准NaOH溶液滴定未知浓度的盐酸,下列说法正确的是( )
| A、本实验可选石蕊作指示剂 |
| B、锥形瓶用水洗净后再用待测液润洗2~3次 |
| C、移液管取盐酸后,垂直放入稍倾斜的锥形瓶中并使管尖与内壁接触 |
| D、滴定过程中眼睛应始终注视滴定管内液面变化 |
下列各组有机物只用一种试剂无法鉴别的是( )
| A、乙醇、乙酸、乙酸乙酯 |
| B、苯酚、己烯、四氯化碳 |
| C、对二甲苯、苯、环己烷 |
| D、乙醛、乙酸、葡萄糖 |
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:下列叙述正确的是( )
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1. 实验测得起始、平衡时的有关数据如下表:
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1. 实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质的物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
| A、反应的速率:③>①>② |
| B、达到平衡时氨气的浓度:①>② |
| C、放出的热量(kJ):a<b<92.4 |
| D、反应得到1mol NH3(l),放出热量46.2kJ |
能把Na2SO4、NH4NO3、(NH4)2SO4、KOH四瓶无色溶液加以区别(必要时可以加热)的一种试剂是( )
| A、BaCl2溶液 |
| B、NaOH溶液 |
| C、AgNO3溶液 |
| D、Ba(OH)2溶液 |
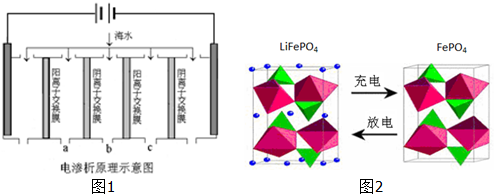
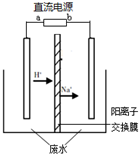 电解CH3CHO是有毒物质,易溶于水,含高浓度CH3CHO的废水可以用隔膜电解法处理,总反应为:
电解CH3CHO是有毒物质,易溶于水,含高浓度CH3CHO的废水可以用隔膜电解法处理,总反应为: