题目内容
18. (1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:
(1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:aA (g)+bB (g)?2C(g)
| 起始物质的量浓度(mol/L) | 1.5 | 1 | 0 |
| 2s末物质的量浓度(mol/L) | 0.9 | 0.8 | 0.4 |
②0到2s用物质B来表示的反应速率为0.1mol/(L•s);
③从反应开始到2s末,A的转化率为40%;
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是BE.
A.vB(反应)=vC(生成) B.容器内气体的总压强保持不变
C.容器内气体的密度不变 D.vA:vB:vC=3:2:2
E.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应式是:2Zn+O2=2ZnO.则该电池的负极材料是锌;
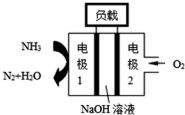
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图,该燃料电池工作时,电池的总反应为4NH3+3O2=2N2+6H2O;负极的电极反应为2NH3-6e-+6OH-═N2+6H2O.
分析 (1)①依据转化量之比等于方程式计算系数之比判断方程式系数书写方程式;
②依据V=$\frac{△C}{△t}$计算;
③α=$\frac{△C}{C0}$×100%;
④根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(2)①原电池负极发生氧化反应;
②在燃料电池的负极上发生燃料氨气失电子的氧化反应,则碱性环境下电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O,电池的总反应为4NH3+3O2=2N2+6H2O.
解答 解:(1)①aA (g)+bB (g)?2C(g)
起始物质的量浓度(mol/L) 1.5 1 0
转化的物质的量浓度(mol/L) 0.6 0.2 0.4
2s末物质的量浓度(mol/L) 0.9 0.8 0.4
依据转化量之比等于方程式计算系数之比,所以反应的方程式:3A (g)+B (g)?2C(g);
故答案为:3A (g)+B (g)?2C(g);
②0到2s用物质B来表示的反应速率为:V(B)=$\frac{0.2mol/L}{2s}$=0.1 mol/(L•s);
故答案为:0.1 mol/(L•s);
③从反应开始到2s末,A的转化率为:$\frac{0.6mol/L}{1.5mol/L}$×100%=40%;
故答案为:40%;
④A.vB(反应)=vC(生成),同种物质的正逆反应速率不等,不是平衡状态,故不选;
B.容器内气体的总压强保持不变,各物质的物质的量不变,为平衡状态,故选;
C.质量、体积均不变,容器内气体的密度始终不变,不能判定平衡状态,故不选;
D.vA:vB:vC=3:2:2始终存在,不能判定平衡状态,故不选;
E.容器内气体C的物质的量分数保持不变,为平衡状态,故选;
故答案为:BE;
(2)①2Zn+O2=2ZnO中锌化合价升高发生氧化反应,所以该电池的负极材料是锌;
故答案为:锌;
②在燃料电池的负极上发生燃料氨气失电子的氧化反应,则碱性环境下电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O②在燃料电池的负极上发生燃料氨气失电子的氧化反应,则碱性环境下电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O,电池的总反应为4NH3+3O2=2N2+6H2O,故答案为:4NH3+3O2=2N2+6H2O;2NH3-6e-+6OH-═N2+6H2O.
点评 本题考查了反应速率、转化率计算,化学平衡状态的判断,燃料电池电极反应式的书写,题目综合性较强,难度中等.

| A. | c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-) | B. | c(Na+)>c(HS-)>c(S2-)>c(H+)>c(OH-) | ||
| C. | c(Na+)>c(HS-)+c(S2-)+c( H2S) | D. | c(HS-)+c(S2-)+c(H2S)=1.0mol•L-1 |
 一定温度下,在三个体积都为2L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)
一定温度下,在三个体积都为2L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O | ||
| Ⅰ | 390 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 390 | |||
| Ⅲ | 230 | 0.20 | 0.090 | 0.090 |
(1)反应的△H<O (填“>”或“<”);判断的理由是投料量相同时,温度高的容器,平衡时二甲醚的物质的量大,说明反应为放热反应,△H小于0.容器I到达平衡所需的时间为20s,反应速率v(CH3OH)为0.004mol/(L•s).390℃时该反应的平衡常数K1=4(填数值).
(2)容器II达平衡时,压强是容器I的两倍,CH3OH的体积分数和容器I中的相同,CH3OH起始的物质的量为0.40mol;平衡时CH3OH(g)的体积分数为20%.
(3)t分钟后容器III达到平衡,t>20s(填“>”“<”或“=”).判断的理由是甲醇的起始浓度相同,但容器I的温度大于容器III的温度.
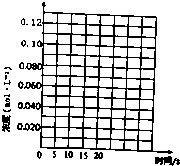
请在图中分别画出容器I和容器III中CH3OH(g)浓度变化的曲线示意图.
(4)390℃,若向3L容器中充入0.9mol CH3OH(g),0.6mol CH3OCH3(g)和0.3molH2O(g),则起始时该反应速率V正>V逆.(填“>”“<”或“=”)
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.相关数据如表:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
②若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是0.03mol/(L•s).
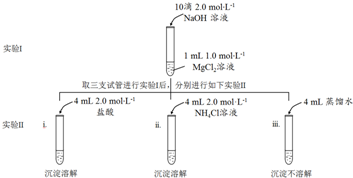
(2)治理汽车尾气的反应是2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0.在恒温恒容的密闭容器中通入n (NO):n(CO)=1:2的混合气体,发生上述反应.下列图象正确且能说明反应在进行到t1时刻一定达到平衡状态的是cd(选填字母).

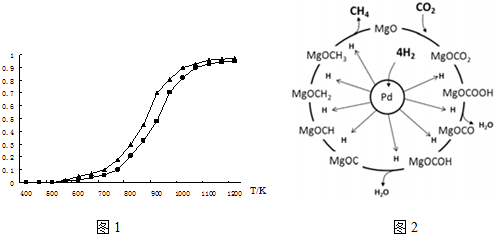
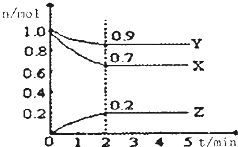 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的两随时间的变化曲线如图所示,据此回答:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的两随时间的变化曲线如图所示,据此回答: