题目内容
下列离子方程式书写正确的是( )
| A、在碘化亚铁溶液中通入足量氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- | ||||
B、用铜电极电解氯化钠饱和溶液:2Cl-+2H2O
| ||||
| C、向硫酸亚铁溶液中通入H2S气体:Fe2++H2S=FeS↓+2H+ | ||||
| D、硫酸亚铁酸性溶液中加入过氧化氢:4Fe2++2H2O2+4H+=4Fe3++4H2O |
考点:离子方程式的书写
专题:
分析:A.氯气足量反应生成氯化铁和碘;
B.Cu电极做阳极,为活性电极,则阳极上Cu失去电子;
C.FeS溶于酸;
D.硫酸亚铁酸性溶液中加入过氧化氢发生氧化还原反应,二价铁被氧化成三价铁.
B.Cu电极做阳极,为活性电极,则阳极上Cu失去电子;
C.FeS溶于酸;
D.硫酸亚铁酸性溶液中加入过氧化氢发生氧化还原反应,二价铁被氧化成三价铁.
解答:
解:A.在碘化亚铁溶液中通入足量氯气,离子方程式:3Cl2+2Fe2++4I-=6Cl-+2Fe3++2I2,故A错误;
B.用铜电极电解食盐水,离子方程式:Cu+2H2O
H2↑+Cu(OH)2↓,故B错误;
C.硫酸亚铁溶液中通入硫化氢不发生反应,故C错误;
D.硫酸亚铁酸性溶液中加入过氧化氢,离子方程式:4Fe2++2H2O2+4H+=4Fe3++4H2O,故D正确;
故选:D.
B.用铜电极电解食盐水,离子方程式:Cu+2H2O
| ||
C.硫酸亚铁溶液中通入硫化氢不发生反应,故C错误;
D.硫酸亚铁酸性溶液中加入过氧化氢,离子方程式:4Fe2++2H2O2+4H+=4Fe3++4H2O,故D正确;
故选:D.
点评:本题考查了离子方程式的书写方法和正误判断,明确反应的实质是解题关键,注意电荷守恒、反应物用量对反应的影响,选项A为易错选项.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列防止金属腐蚀的做法不可行的是( )
| A、自行车的钢圈和车铃上镀上一层铬,既耐腐蚀又美观耐磨 |
| B、衣架和电线外面包上一层塑料层以防锈 |
| C、在钢材制造的大型船舶上装上一定数量的锌块 |
| D、在某些工具的机械转动部位刷油漆以防锈 |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、标准状况下,边长为28.2cm(内空)的立方体容器内所盛有的N2的分子数目约为NA |
| B、在熔融状态下,l mol NaHSO4完全电离出的阳离子数目为2NA |
| C、7.8 g Na2O2含有的阴离子数目为0.2 NA |
| D、标准状况下,22.4L庚烷完全燃烧生成的CO2分子数目为7NA |
现榨的苹果汁在空气中会由淡绿色变为棕黄色,其原因可能是( )
| A、苹果汁中的Fe2+变成Fe3+ |
| B、苹果汁中含有Cu2+ |
| C、苹果汁含有Cl- |
| D、苹果汁含有Na+ |
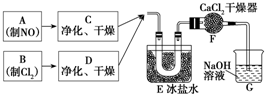 亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到(NO2与Cl2反应可得硝酰氯).亚硝酰氯的熔点为-64.5℃,沸点为-5.5℃,并且遇水蒸气分解为氮的氧化物和氯化氢.
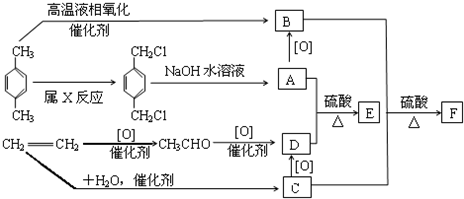
亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到(NO2与Cl2反应可得硝酰氯).亚硝酰氯的熔点为-64.5℃,沸点为-5.5℃,并且遇水蒸气分解为氮的氧化物和氯化氢.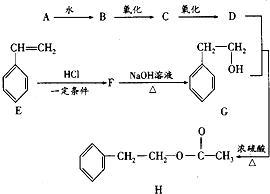 乙酸苯乙酯是一种具有玫瑰花香,并带有可可香韵的有机物,常用于调配玫瑰、橙花、紫罗兰、晚香玉、野蔷薇等香精.天然乙酸苯乙酯存在于白兰花油和玫瑰花油中,也可通过化学方法合成.如图是一种合成路线(部分反应物和条件省略).
乙酸苯乙酯是一种具有玫瑰花香,并带有可可香韵的有机物,常用于调配玫瑰、橙花、紫罗兰、晚香玉、野蔷薇等香精.天然乙酸苯乙酯存在于白兰花油和玫瑰花油中,也可通过化学方法合成.如图是一种合成路线(部分反应物和条件省略).