题目内容
下列对应微粒的电子式书写正确的是( )
分析:A、简单阳离子的电子式为其离子符号;
B、在元素符号周围用小黑点“?”或小叉“×”来表示元素原子的最外层电子;
C、阴离子、复杂阳离子电子式用[],并在右上角注明所带电荷;
D、中性原子既没有得电子,也没有失电子,所以书写电子式时应把原子的最外层电子全部排列在元素符号周围.排列方式为在元素符号上、下、左、右四个方向,每个方向不能超过2个电子.
B、在元素符号周围用小黑点“?”或小叉“×”来表示元素原子的最外层电子;
C、阴离子、复杂阳离子电子式用[],并在右上角注明所带电荷;
D、中性原子既没有得电子,也没有失电子,所以书写电子式时应把原子的最外层电子全部排列在元素符号周围.排列方式为在元素符号上、下、左、右四个方向,每个方向不能超过2个电子.
解答:解:A、简单阳离子的电子式为其离子符号,钾离子电子式为K+,故A错误;
B、氦原子He有2个电子,为稳定结构,电子式为He:,不能将2个电子分开,故B正确;
C、氯离子是阴离子,带1个单位负电荷,电子式为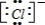 ,故C错误;
,故C错误;
D、锂原子最外层1个电子,电子式为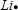 ,故D错误.
,故D错误.
故选B.
B、氦原子He有2个电子,为稳定结构,电子式为He:,不能将2个电子分开,故B正确;
C、氯离子是阴离子,带1个单位负电荷,电子式为
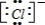 ,故C错误;
,故C错误;D、锂原子最外层1个电子,电子式为
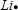 ,故D错误.
,故D错误.故选B.
点评:本题考查电子式的书写,难度较小,注意铵根离子、水合氢离子、氢氧根、过氧根离子的电子式书写.B中氦的2个电子不能拆开,与镁原子不同,可结合性质理解.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
下列对应微粒的电子式书写正确的是( )
A.钾离子 | B.氦原子He∶ |
| C.氯离子Cl- | D.锂原子·Li∶ |
 B.氦原子He∶
B.氦原子He∶
