题目内容
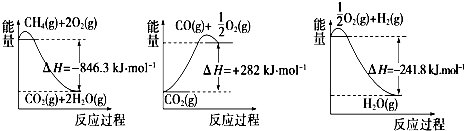
11.氨是最重要的化工产品之一.(1)合成氨用的氢气可以甲烷为原料制得:CH4(g)+H2O(g)?CO(g)+3H2(g).有关化学反应的能量变化如图所示.CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为CH4(g)+H2O(g)=CO(g)+3H2 (g)△H=+161.1kJ•mol-1.
(2)CO对合成氨的催化剂有毒害作用,常用乙酸二氨合铜(Ⅰ)溶液来吸收原料气中CO,其反应原理为[Cu(NH3)2CH3COO](l)+CO(g)+NH3(g)?[Cu(NH3)3]CH3COO•CO(l)△H<0.吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,再生的适宜条件是B.(填字母)
A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
(3)用氨气制取尿素[CO(NH2)2]的反应为2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g)△H<0.某温度下,向容积为100L的密闭容器中通入4molNH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%.该温度下此反应平衡常数K的值为2500 L2•mol-2.
(4)将尿素施入土壤后,大部分是通过转化为碳酸铵或碳酸氢铵后才被作物所利用,尿素分子在微生物分泌的脲酶作用下,转化为碳酸铵.已知弱电解质在水中的电离平衡常数(25℃)如表:现有常温下0.1mol•L-1的(NH4)2CO3溶液,
| 弱电解质 | H2CO3 | NH3•H2O |
| Ka1 | 4.30×10-7 | 1.77×10-5 |
| Ka2 | 5.61×10-11 |
②就该溶液中粒子之间有下列关系式,你认为其中不正确的是B.
A.c(NH4+)>c(CO32-)>c(HCO3-)>c(NH3•H3O)
B.c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1
D.c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
分析 (1)由图可得热化学方程式:①CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-846.3KJ/mol
②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-282KJ/mol
③H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8KJ/mol
根据盖斯定律,①-③×3-②得到:CH4(g)+H2O(g)=CO(g)+3H2 (g);
(2)吸收CO后的乙酸铜氨液经过适当处理后又可再生,用使平衡逆向移动,正反应为气体体积减小的放热反应,在高温、低压下有利于平均逆向进行;
(3)某温度下,向容积为100L的密闭容器中通入4molNH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%,转化的二氧化碳为1mol,则:
2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g)
起始量(mol):4 2 0
变化量(mol):2 1 1
平衡量(mol):2 1 1
再根据K=$\frac{c({H}_{2}O)}{{c}^{2}(N{H}_{3})×c(C{O}_{2})}$计算平衡常数;
(4)①电离平衡常数NH3•H2O>H2CO3>HCO3-,水解程度NH4+<HCO3-<CO32-,常温下0.1mol•L-1的(NH4)2CO3溶液呈碱性;
②A.溶液中铵根离子浓度大于碳酸根离子浓度,碳酸根离子水解程度大于铵根离子水解程度;
B.根据电荷守恒判断;
C.根据物料守恒判断;
D.溶液中物料守恒:n(N):n(C)=2:1.
解答 解:(1)由图可得热化学方程式:①CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-846.3KJ/mol
②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-282KJ/mol
③H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8KJ/mol
根据盖斯定律,①-③×3-②得到:CH4(g)+H2O(g)=CO(g)+3H2 (g)△H=+161.1kJ•mol-1,
故答案为:CH4(g)+H2O(g)=CO(g)+3H2 (g)△H=+161.1kJ•mol-1;
(2)吸收CO后的乙酸铜氨液经过适当处理后又可再生,用使平衡逆向移动,正反应为气体体积减小的放热反应,在高温、低压下有利于平均逆向进行,
故选:B;
(3)某温度下,向容积为100L的密闭容器中通入4molNH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%,转化的二氧化碳为1mol,则:
2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g)
起始量(mol):4 2 0
变化量(mol):2 1 1
平衡量(mol):2 1 1
则平衡常数K=$\frac{c({H}_{2}O)}{{c}^{2}(N{H}_{3})×c(C{O}_{2})}$=$\frac{\frac{1}{100}}{(\frac{2}{100})^{2}×\frac{1}{100}}$=2500L2•mol-2,
故答案为:2500 L2•mol-2;
(4)①电离平衡常数NH3•H2O>H2CO3>HCO3-,水解程度NH4+<HCO3-<CO32-,常温下0.1mol•L-1的(NH4)2CO3溶液呈碱性,
故答案为:碱性;
②A.溶液中铵根离子浓度大于碳酸根离子浓度,碳酸根离子水解程度大于铵根离子水解程度,所以溶液中离子浓度大小为:c(NH4+)>c(CO32-)>c(HCO3-)>c(NH3•H2O),故A正确;
B.溶液中存在电荷守恒为:c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-),故B错误;
C.由溶液中物料守恒得到:c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1 ,故C正确;
D.由溶液中物料守恒,n(N):n(C)=2:1,结合溶液中离子种类和守恒关系得到:c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故D正确;
故答案为:B.
点评 本题考查了热化学方程式书写、化学平衡影响因素、平衡常数、离子浓度比较等,是对学生综合能力的考查,(4)中离子浓度比较中注意对物料守恒的理解,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 7.8g Na2O2中含有的阴离子数目为0.2 NA | |
| B. | 0.1mol Fe与足量稀HNO3反应,转移电子数为0.3NA | |
| C. | 1L 0.1 mol/L Al2(SO4)3溶液中,Al3+的数目为0.2 NA | |
| D. | 标准状况下,2.24L CHCl3的分子数为0.1 NA |
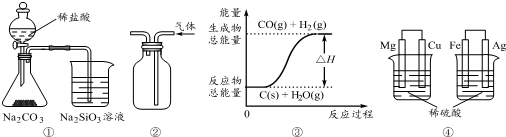
| A. | 用图①所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
| B. | 用图②所示实验装置排空气法收集NO2气体 | |
| C. | 图③表示可逆反应C(s)+H2O(g)?CO(g)+H2(g)的△H小于0 | |
| D. | 图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不相同 |
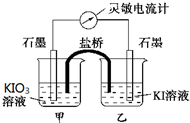 将反应IO3-+5I-+6H+?3I2+3H2O设计成如图所示的原电池,甲、乙烧杯中都加入淀粉溶液.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转.下列判断不正确的是( )
将反应IO3-+5I-+6H+?3I2+3H2O设计成如图所示的原电池,甲、乙烧杯中都加入淀粉溶液.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转.下列判断不正确的是( )| A. | 两次电流计指针偏转方向相反,电流计读数为零时,反应达到化学平衡状态 | |
| B. | 两次实验中,盐桥中的阳离子移动方向相反 | |
| C. | 开始加入少量浓硫酸时,只有乙烧杯中溶液变蓝 | |
| D. | 向甲烧杯中滴入几滴浓NaOH溶液后,乙中石墨电极上发生还原反应 |
| 阳离子 | K+ NH4+ Fe2+ Mg2+ Al3+ Cu2+ |
| 阴离子 | OH- Cl- Al02- CO32- SiO32-SO42- |
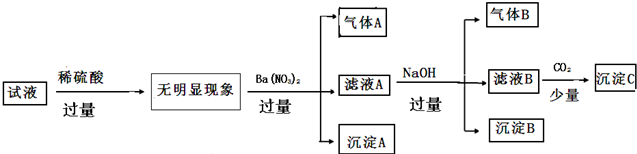
下列说法正确的是( )
| A. | 原溶液中只含有NH4+ Fe2+Cl- SO42- | |
| B. | 由沉淀A推断原溶液中一定含有SO42- | |
| C. | 滤液A中可能含有K+ Al3+ Cl- | |
| D. | 沉淀B中一定含有Mg(OH)2 |
| A. | AgNO3 | B. | NaNO3 | C. | Mg(NO3)2 | D. | Al(NO3)3 |
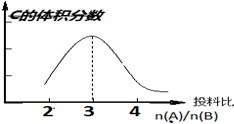 在恒温恒压条件下:aA(g)+bB(g)?2C(g),以不同的投料比开始反应,分别达到平衡时,C的体积分数与投料比的关系如图所示:
在恒温恒压条件下:aA(g)+bB(g)?2C(g),以不同的投料比开始反应,分别达到平衡时,C的体积分数与投料比的关系如图所示:
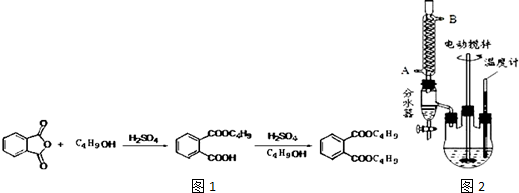
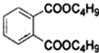 +2NaOH$\stackrel{加热}{→}$
+2NaOH$\stackrel{加热}{→}$ +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.