题目内容
图为周期表中短周期的一部分,若A原子的最外电子层上有5个电子,则下列说法中不正确的是( )

| A.原子半径A>B>C |
| B.B的氢化物比C的氢化物稳定 |
| C.B对应阴离子的还原性比C对应阴离子的还原性强 |
| D.A的最高价氧化物对应水化物比B的最高价氧化物对应水化物的酸性弱 |

A为P元素,B为S元素,C为Cl元素,D为O元素.
A、同周期元素的从左到右原子半径逐渐减小,则A>B>C,故A正确;
B、同周期元素从左到右元素的非金属性逐渐增强,所以非金属性C>B,元素的非金属性越强,氢化物越稳定,所以C的氢化物比B的氢化物稳定,故B错误;
C、同周期元素从左到右元素的非金属性逐渐增强,所以非金属性C>B,元素的非金属性越强,相应阴离子的还原性越弱,即B对应阴离子的还原性比C对应阴离子的还原性强,故C正确;
D、同周期元素从左到右元素的非金属性逐渐增强,所以非金属性B>A,元素的非金属性越强,对应最高价氧化物的水化物的酸性越强,所以最高价氧化物对应水化物的酸性:B>A,故D正确.
故选:B.
A、同周期元素的从左到右原子半径逐渐减小,则A>B>C,故A正确;
B、同周期元素从左到右元素的非金属性逐渐增强,所以非金属性C>B,元素的非金属性越强,氢化物越稳定,所以C的氢化物比B的氢化物稳定,故B错误;
C、同周期元素从左到右元素的非金属性逐渐增强,所以非金属性C>B,元素的非金属性越强,相应阴离子的还原性越弱,即B对应阴离子的还原性比C对应阴离子的还原性强,故C正确;
D、同周期元素从左到右元素的非金属性逐渐增强,所以非金属性B>A,元素的非金属性越强,对应最高价氧化物的水化物的酸性越强,所以最高价氧化物对应水化物的酸性:B>A,故D正确.
故选:B.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
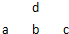 如图为周期表中短周期的一部分,若a原子最外层上有5个电子,则下列说法中不正确的是( )
如图为周期表中短周期的一部分,若a原子最外层上有5个电子,则下列说法中不正确的是( )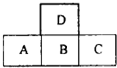 图为周期表中短周期的一部分,若A原子的最外电子层上有5个电子,则下列说法中不正确的是( )
图为周期表中短周期的一部分,若A原子的最外电子层上有5个电子,则下列说法中不正确的是( ) 右图为周期表中短周期的一部分,若A原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )
右图为周期表中短周期的一部分,若A原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )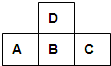 如图为周期表中短周期的一部分,若A原子的最外电子层上有5个电子,则下列说法中不正确的是( )
如图为周期表中短周期的一部分,若A原子的最外电子层上有5个电子,则下列说法中不正确的是( )