题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、在标准状况下,11.2L 氦气含有NA个氦原子 |
| B、25℃,1.01×105Pa,64gSO2中含有的原子数为3NA |
| C、11.2L CO含有的分子数为0.5NA |
| D、1mol氧分子含有的电子数与1mol氮气含有的电子数之比为16:7 |
考点:阿伏加德罗常数
专题:
分析:A.氦气是由单原子构成的分子;
B.64g二氧化硫的物质的量是1mol;
C.不一定是标准状况下;
D.1mol氧气中含有16mol电子,1mol氮气中含有14mol电子.
B.64g二氧化硫的物质的量是1mol;
C.不一定是标准状况下;
D.1mol氧气中含有16mol电子,1mol氮气中含有14mol电子.
解答:
解:A.氦气是由单原子构成的分子,11.2L 氦气的物质的量是1mol,含有0.5NA个氦原子,故A错误;
B.64g二氧化硫的物质的量是1mol,含有3mol原子,含有的原子数为3NA,故B正确;
C.不一定是标准状况下,无法计算CO的物质的量,故C错误;
D.1mol氧分子含有16mol电子,1mol氮气含有14mol电子,二者含有的电子数之比为16:14=8:7,故D错误.
故选B.
B.64g二氧化硫的物质的量是1mol,含有3mol原子,含有的原子数为3NA,故B正确;
C.不一定是标准状况下,无法计算CO的物质的量,故C错误;
D.1mol氧分子含有16mol电子,1mol氮气含有14mol电子,二者含有的电子数之比为16:14=8:7,故D错误.
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下水不是气体.

练习册系列答案
相关题目
金属铜制取硝酸铜,从节约原料和防止环境污染考虑,最好的方法是( )
A、铜
| ||||
B、铜
| ||||
C、铜
| ||||
D、铜
|
关于居室内空气污染的说法错误的是( )
| A、居室内空气中存在的污染物主要来自于装修材料、日用化学品、香烟烟雾以及家用燃料的燃烧产物等 |
| B、燃料不完全燃烧产生的一氧化碳也是一种室内污染物 |
| C、在居室内放置几盒花草就可消除室内空气污染 |
| D、预防装修污染,最重要的是选择经过严格检测的、环保的装修材料 |
20g密度为dg/cm3的硝酸钙溶液中,含有lgCa2+,则NO3-的物质的量浓度为( )
| A、mol/L |
| B、mol/L |
| C、2.5dmol/L |
| D、1.25dmol/L |
某溶液X含有K+、Mg2+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-中的几种,已知该溶液中各离子物质的量浓度均为0.1mol?L-1(不考虑水的电离及离子的水解).为确定该溶液中含有的离子,现进行了如下的操作:下列说法正确的是( )
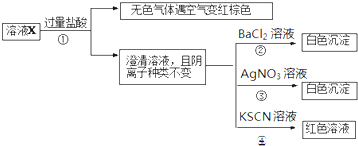

| A、无色气体可能是NO和CO2的混合物 |
| B、由步骤③可以确定原溶液中含有Cl- |
| C、溶液X中所含离子种类共有4种 |
| D、另取l00mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为1.2g |