题目内容
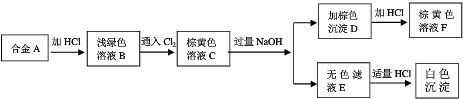
稀土是工业味精,邓小平说过“中东有石油,我们有稀土”.稀土元素铈(Ce)主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应.已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+.下列说法正确的是( )
| A、已知Ce原子序数是58,则其为镧系元素 | ||||||||
B、铈有四种稳定的核
| ||||||||
| C、用Ce(SO4)2溶液可与硫酸亚铁溶液反应,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+ | ||||||||
| D、铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑ |
考点:氧化还原反应,同位素及其应用
专题:
分析:A.镧系元素是第57号元素镧到71号元素镥15种元素的统称;
B.质子数相同而中子数不同的一类原子互称为同位素;
C.电荷不守恒;
D.由Fe3+氧化I-可知,Ce4+也可氧化I-,故CeI4不存在,应为CeI3.
B.质子数相同而中子数不同的一类原子互称为同位素;
C.电荷不守恒;
D.由Fe3+氧化I-可知,Ce4+也可氧化I-,故CeI4不存在,应为CeI3.
解答:
解:A.镧系元素是第57号元素镧到71号元素镥15种元素的统称,则Ce原子序数是58,则其为镧系元素,故A正确;
B.
Ce、
Ce、
Ce、
Ce质子数均Wie58,中子数不同,则互称为同位素,故B正确;
C.用Ce(SO4)2溶液可与硫酸亚铁溶液反应,其离子方程式为Ce4++Fe2+=Ce3++Fe3+,故C错误;
D.由Fe3+氧化I-可知,Ce4+也可氧化I-,故CeI4不存在,应为CeI3,则铈溶于氢碘酸的化学方程式可表示为:2Ce+6HI=2CeI3+3H2↑,故D错误;
故选AB.
B.
136 58 |
138 58 |
140 58 |
142 58 |
C.用Ce(SO4)2溶液可与硫酸亚铁溶液反应,其离子方程式为Ce4++Fe2+=Ce3++Fe3+,故C错误;
D.由Fe3+氧化I-可知,Ce4+也可氧化I-,故CeI4不存在,应为CeI3,则铈溶于氢碘酸的化学方程式可表示为:2Ce+6HI=2CeI3+3H2↑,故D错误;
故选AB.
点评:本题考查氧化还原反应,为高频考点,把握相关概念及元素的化合价变化、离子反应的书写等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
在酸性无色溶液中,可以大量共存的离子组是( )
| A、K+、Na+、Cl-、CO32- |
| B、Cu2+、Cl-、Na+、SO42- |
| C、Ca2+、Na+、Cl-、NO3- |
| D、Fe3+、NH4+、SCN-、HCO3-、 |
有甲、乙两个完全相同的装置如图,某学生分别在它们的侧管中装入0.01mol Na2CO3和0.01molNaHCO3,甲、乙中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
Na2CO3和0.01molNaHCO3,甲、乙中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
 Na2CO3和0.01molNaHCO3,甲、乙中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
Na2CO3和0.01molNaHCO3,甲、乙中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )| A、最终两试管中Na+、Cl-的物质的量一定相同 |
| B、甲装置的气球膨胀速率大 |
| C、若最终两气球体积不同,则盐酸的浓度一定小于或等于1mol/L |
| D、若最终两气球体积相同,则盐酸的浓度一定大于或等于2mol/L |
 .如图所示是九种化合物的转变关系.
.如图所示是九种化合物的转变关系.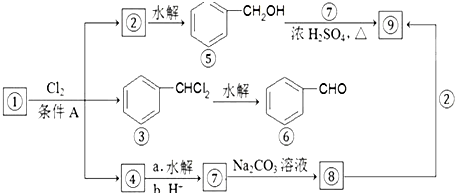
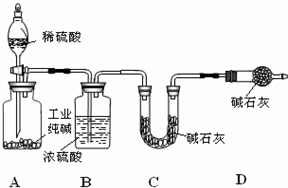 工业纯碱中常含有NaCl、Na2SO4杂质,为了测定工业纯碱中Na2CO3的含量,某同学设计了如图装置:
工业纯碱中常含有NaCl、Na2SO4杂质,为了测定工业纯碱中Na2CO3的含量,某同学设计了如图装置: