题目内容
一定条件下在固定容积的密闭容器中生产尿素的反应如下:
CO2(g)+2NH3(g)═CO(NH2)2(s)+H2O(g),
(1)该反应的平衡常数表达式为
(2)根据图1判断,该反应的正反应属于 (填“吸热”或“放热”)反应;升高温度,该混合气体的密度将 (填“增大”“减小”或“不变”).
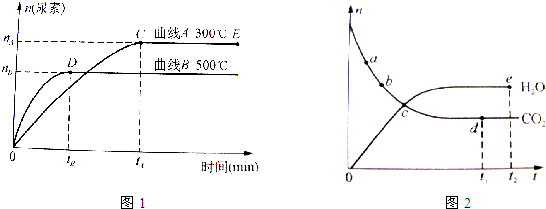
(3)图2表示某温度时某些物质的物质的量(n)随时间(t)变化的关系.
①图中达到平衡的点是 (填“a、b、c、d、e”).
②v(CO2)正反应速率:a点 b点; n(NH3):d 点 e点 (填“>”“<”或“=”).
③在其他条件不变的情况下,向处于t2时刻的体系中再充入一定量的CO2(g),下列说法正确的是 .
A.NH3的转化率增大 B.正反应速率加快,逆反应速率减慢
C.平衡常数K值增大 D.重新达到平衡时,n(NH3)/n(H2O)减小.
CO2(g)+2NH3(g)═CO(NH2)2(s)+H2O(g),
(1)该反应的平衡常数表达式为
(2)根据图1判断,该反应的正反应属于

(3)图2表示某温度时某些物质的物质的量(n)随时间(t)变化的关系.
①图中达到平衡的点是
②v(CO2)正反应速率:a点
③在其他条件不变的情况下,向处于t2时刻的体系中再充入一定量的CO2(g),下列说法正确的是
A.NH3的转化率增大 B.正反应速率加快,逆反应速率减慢
C.平衡常数K值增大 D.重新达到平衡时,n(NH3)/n(H2O)减小.
考点:化学平衡常数的含义,化学平衡的影响因素,物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)依据化学方程式和平衡常数概念书写平衡常数表达式;
(2)图象可知,温度越高尿素物质的量越小,说明升温平衡逆向进行,正反应为放热反应,反应前后气体质量变化,体积不变,升高温度平衡逆向进行气体质量增大,该混合气体的密度增大;
(3)①反应达到平衡状态的标志是正逆反应速率相同,某种气体物质的物质的量不变说明反应达到平衡;
②ab点二氧化碳的反应速率依据气体物质的量大小比较,物质的量越大,浓度越大,反应速率越大,de点是平衡状态,氨气的物质的量相同;
③依据化学平衡移动原理分析选项,CO2(g)+2NH3(g)═CO(NH2)2(s)+H2O(g),反应是气体体积减小的放热反应,向处于t2时刻的体系中再充入一定量的CO2(g);
A.两种反应物,增加一种物质会提高另一种物质的转化率;
B.增大反应物浓度,反应速率增大,正逆反应速率都增大;
C.平衡常数K值随温度变化,不随浓度改变;
D.平衡正向进行,重新达到平衡时,n(NH3)/n(H2O)减小;
(2)图象可知,温度越高尿素物质的量越小,说明升温平衡逆向进行,正反应为放热反应,反应前后气体质量变化,体积不变,升高温度平衡逆向进行气体质量增大,该混合气体的密度增大;
(3)①反应达到平衡状态的标志是正逆反应速率相同,某种气体物质的物质的量不变说明反应达到平衡;
②ab点二氧化碳的反应速率依据气体物质的量大小比较,物质的量越大,浓度越大,反应速率越大,de点是平衡状态,氨气的物质的量相同;
③依据化学平衡移动原理分析选项,CO2(g)+2NH3(g)═CO(NH2)2(s)+H2O(g),反应是气体体积减小的放热反应,向处于t2时刻的体系中再充入一定量的CO2(g);
A.两种反应物,增加一种物质会提高另一种物质的转化率;
B.增大反应物浓度,反应速率增大,正逆反应速率都增大;
C.平衡常数K值随温度变化,不随浓度改变;
D.平衡正向进行,重新达到平衡时,n(NH3)/n(H2O)减小;
解答:
解:(1)CO2(g)+2NH3(g)═CO(NH2)2(s)+H2O(g),反应的平衡常数为K=
;
故答案为:
;
(2)根据图1判断,温度越高尿素物质的量越小,说明升温平衡逆向进行,正反应为放热反应,反应前后气体质量变化,体积不变,升高温度平衡逆向进行气体质量增大,该混合气体的密度增大;
故答案为:放热,增大;
(3)①达到平衡状态的标志是正逆反应速率相同,图象中de点二氧化碳和水的物质的量不变,说明反应达到平衡状态;
故答案为:d、e;
②图象中a点二氧化碳物质的量大于b点二氧化碳物质的量,说明a点浓度大反应速率大,氨气物质的量n(NH3)在de点是爱反应达到的平衡状态,所以氨气物质的量是相同的;
故答案为:>,=;
③向处于t2时刻的体系中再充入一定量的CO2(g),CO2(g)+2NH3(g)═CO(NH2)2(s)+H2O(g),反应是气体体积减小的放热反应;
A.两种反应物,增加一种物质会提高另一种物质的转化率,增加二氧化碳会提高NH3的转化率,故A正确;
B.增大反应物浓度,反应速率增大,正逆反应速率都增大,故B错误;
C.平衡常数K值随温度变化,不随浓度改变,故C错误;
D.平衡正向进行,重新达到平衡时,氨气物质的量减小,水物质的量增大,所以n(NH3)/n(H2O)减小,故D正确;
故答案为:A D;
| c(H2O) |
| c(CO2)c2(NH3) |
故答案为:
| c(H2O) |
| c(CO2)c2(NH3) |
(2)根据图1判断,温度越高尿素物质的量越小,说明升温平衡逆向进行,正反应为放热反应,反应前后气体质量变化,体积不变,升高温度平衡逆向进行气体质量增大,该混合气体的密度增大;
故答案为:放热,增大;
(3)①达到平衡状态的标志是正逆反应速率相同,图象中de点二氧化碳和水的物质的量不变,说明反应达到平衡状态;
故答案为:d、e;
②图象中a点二氧化碳物质的量大于b点二氧化碳物质的量,说明a点浓度大反应速率大,氨气物质的量n(NH3)在de点是爱反应达到的平衡状态,所以氨气物质的量是相同的;
故答案为:>,=;
③向处于t2时刻的体系中再充入一定量的CO2(g),CO2(g)+2NH3(g)═CO(NH2)2(s)+H2O(g),反应是气体体积减小的放热反应;
A.两种反应物,增加一种物质会提高另一种物质的转化率,增加二氧化碳会提高NH3的转化率,故A正确;
B.增大反应物浓度,反应速率增大,正逆反应速率都增大,故B错误;
C.平衡常数K值随温度变化,不随浓度改变,故C错误;
D.平衡正向进行,重新达到平衡时,氨气物质的量减小,水物质的量增大,所以n(NH3)/n(H2O)减小,故D正确;
故答案为:A D;
点评:本题考查了化学平衡常数影响因素和计算分析应用,图象分析和平衡标志是关键,题目难度中等.

练习册系列答案
相关题目
研究物质变化时,人们可以从不同的角度、不同的层面来认识物质变化时所引起的化学键及能量变化.据此判断以下叙述中错误的是( )
| A、金属钠与氯气反应生成氯化钠后,稳定性增强,体系的能量降低 |
| B、物质燃烧可看成“储存”在物质内部的能量(化学能)转化为热能释放出来 |
| C、氮分子内部存在着很强的共价键,故通常状况下氮气的化学性质很不活泼 |
| D、需加热才能发生的反应一定是吸收能量的反应 |
下列能用勒沙特列原理解释的是( )
| A、加入催化剂后H2和O2反应生成水 |
| B、棕红色NO2加压后颜色先变深后变浅 |
| C、SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D、H2、I2、HI平衡混和气加压后颜色变深 |
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.