题目内容
单质硫在NaOH的热溶液中发生歧化反应:3S+6NaOH→2Na2S+Na2SO3+3H2O,若硫过量,进一步生成Na2Sx(x≤5)和Na2S2O3,将2.56g硫与含0.06molNaOH的热溶液充分反应恰好生成amolNa2S3和bmol Na2S2O3,再加入足量NaClO-NaOH的混合溶液,硫元素全部转化为Na2SO4,转移电子n mol,则以下正确的是( )
| A、a=2b |
| B、2a=b |
| C、n=0.48 |
| D、b=0.02 |
考点:氧化还原反应的计算
专题:
分析:2.56g硫单质的物质的量为:
=0.08mol;同一氧化还原反应中转移电子数相等,且反应前后各元素的原子个数相等,根据电子守恒和质量守恒定律进行计算.
| 2.56g |
| 32g/mol |
解答:
解:2.56g硫单质的物质的量为:
=0.08mol,将0.08mol单质硫与含0.06mol NaOH的热溶液充分反应恰好生成a mol Na2Sx和b mol Na2S2O3,根据硫原子、Na原子守恒和转移电子守恒得:2a+2b=0.06、ax+2b=0.08、2a=2×b×(2-0),解得:x=3、a=0.02、b=0.01,所以A正确、BD错误;
再加入足量NaClO、NaOH的混合溶液,硫元素全部转化为Na2SO4,转移电子n mol,实际上转移电子总数为硫单质转化为硫酸根离子失去的电子数,n=0.08mol×(6-0)=0.48mol,故C正确;
故选AC.
| 2.56g |
| 32g/mol |
再加入足量NaClO、NaOH的混合溶液,硫元素全部转化为Na2SO4,转移电子n mol,实际上转移电子总数为硫单质转化为硫酸根离子失去的电子数,n=0.08mol×(6-0)=0.48mol,故C正确;
故选AC.
点评:本题考查了氧化还原反应的计算,根据氧化还原反应中原子守恒、转移电子相等进行计算即可,注意硫代硫酸钠中其中一个硫原子的化合价为-2价,可以采用平均化合价的方法判断硫代硫酸钠中硫元素的化合价,硫元素的平均化合价为+2价,为易错点.

练习册系列答案
相关题目
下列溶液中NO3-的物质的量最大的是( )
| A、500 mL 1 mol/L的KNO3溶液 |
| B、500 mL 1 mol/L的Ba(NO3)2溶液 |
| C、100 mL 0.5 mol/L的Mg(NO3)2溶液 |
| D、1 L 0.5 mol/L的Fe(NO3)3溶液 |
某种类型的心脏起搏器工作时发生下列反应:4Li+2SOCl2=4LiCl+S+SO2.下列有关判断正确的是( )
| A、还原剂只有锂 |
| B、SOCl2中既有离子键,也有共价键 |
| C、氧化产物包括LiCl和SO2 |
| D、标准状况下生成1.12LSO2时,反应转移电子为0.1mol |
铟产业被称为“信息时代的朝阳产业”.元素周期表中铟的数据见图,下列说法完全正确的是( )


| A、铟元素的质量数是114.8 |
| B、铟元素的相对原子质量是115,中子数为66 |
| C、铟元素是一种主族元素,位于第五周期第ⅢA族 |
| D、铟原子最外层有3个能量相同的电子 |
0.03molCu投入到一定量的浓HNO3 中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2 的体积为( )
| A、504mL |
| B、336mL |
| C、224mL |
| D、168mL |
设NA为阿伏加德罗常数的数值,下列说法错误的是( )
| A、已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1,当有3NA个电子转移时,△H变为-46.2kJ?mol-1 |
| B、1mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数NA个 |
| C、2.9g熟石膏(2CaSO4?H2O)含有的结晶水分子数为0.01NA个 |
| D、由1mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 |
下列有机物命名正确的是( )
A、 2-乙基丙烷 2-乙基丙烷 |
B、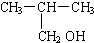 2-甲基丙醇 2-甲基丙醇 |
C、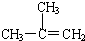 2-甲基丙烯 2-甲基丙烯 |
D、 2,2-二甲基-3-丁醇 2,2-二甲基-3-丁醇 |