题目内容
在一只小烧杯里,加入20g Ba(OH)2?8H2O粉末,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后加入10g NH4+Cl晶体,并用玻璃棒迅速搅拌.
(1)实验中玻璃棒的作用是
(2)写出有关反应的化学方程式: 该反应属 反应(填基本反应类型).
(3)实验中观察到的现象有 、 且反应混合物成糊状,反应混合物呈糊状的原因是 .
(4)通过 现象,说明该反应为 热反应,这是由于反应物的总能量 生成物的总能量.
(1)实验中玻璃棒的作用是
(2)写出有关反应的化学方程式:
(3)实验中观察到的现象有
(4)通过
考点:探究吸热反应和放热反应
专题:化学反应中的能量变化
分析:(1)固体混合物的反应用玻璃棒搅拌有利于充分接触,加速反应进行;
(2)反应为复分解反应,二者反应生成氨气、水、以及氯化钡;根据该反应特点判断反应类型;
(3)氯化铵铵盐和强碱氢氧化钡的反应生成氨气、水、以及氯化钡,以此解释反应现象;
(4)玻璃片上结冰而与小烧杯粘在一起,说明氢氧化钡和氯化铵的反应是吸热反应,反应物的总能量小于生成物的总能量.
(2)反应为复分解反应,二者反应生成氨气、水、以及氯化钡;根据该反应特点判断反应类型;
(3)氯化铵铵盐和强碱氢氧化钡的反应生成氨气、水、以及氯化钡,以此解释反应现象;
(4)玻璃片上结冰而与小烧杯粘在一起,说明氢氧化钡和氯化铵的反应是吸热反应,反应物的总能量小于生成物的总能量.
解答:
(1)玻璃棒在化学实验中的作用:搅拌和引流,本实验中,根据题意:将20g Ba(OH)2?8H2O晶体与10g NH4Cl晶体一起放入小烧杯中,将烧杯放在滴有3~4滴水的玻璃片上,用玻璃棒迅速搅拌,可以知道玻璃棒的作用是:搅拌使混合物充分接触并反应,
故答案为:搅拌使混合物充分接触并反应;
(2)氯化铵属于铵盐,能和强碱氢氧化钡反应生成氨气、水、以及氯化钡,化学方程式为Ba(OH)2?8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O,该反应属于复分解反应,
故答案为:Ba(OH)2?8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;复分解;
(3)氯化铵铵盐和强碱氢氧化钡的反应是吸热反应,温度降低能让水结冰,导致烧杯和玻璃片粘在一起,同时生成的氨气具有刺激性气味,反应混合物成糊状,原因是反应过程中生成水的缘故,
故答案为:玻片与烧杯之间结冰黏在一起;有少许刺激性气味的气体;反应过程中有水生成;
(4)玻璃片上结冰而与小烧杯粘在一起,说明氢氧化钡和氯化铵的反应是吸热反应,即反应物的总能量小于生成物的总能量,
故答案为:结冰;吸;小于.
故答案为:搅拌使混合物充分接触并反应;
(2)氯化铵属于铵盐,能和强碱氢氧化钡反应生成氨气、水、以及氯化钡,化学方程式为Ba(OH)2?8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O,该反应属于复分解反应,
故答案为:Ba(OH)2?8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;复分解;
(3)氯化铵铵盐和强碱氢氧化钡的反应是吸热反应,温度降低能让水结冰,导致烧杯和玻璃片粘在一起,同时生成的氨气具有刺激性气味,反应混合物成糊状,原因是反应过程中生成水的缘故,
故答案为:玻片与烧杯之间结冰黏在一起;有少许刺激性气味的气体;反应过程中有水生成;
(4)玻璃片上结冰而与小烧杯粘在一起,说明氢氧化钡和氯化铵的反应是吸热反应,即反应物的总能量小于生成物的总能量,
故答案为:结冰;吸;小于.
点评:本题考查吸热反应的探究,题目难度不大,本题注意把握氯化铵和氢氧化钡反应的原理,注意从反应物与生成物总能量的关系分析.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
X、Y、Z、R、Q为元素周期表前20号的五种主族元素,且原子半径依次减小,其中X和Q同主族,X与Z、Y与Q原子的电子层数都相差2,X、Y原子最外层电子数之比为1:4,Z的最外层电子数是次外层的3倍.下列说法不正确的是( )
| A、Y和Z形成的某种化合物具有空间网状结构 |
| B、X和Z可形成X2Z、X2Z2的化合物 |
| C、R和Q形成的化合物含有共价键且为强电解质 |
| D、X的失电子能力比Q强 |
已知HCl气体极易溶于水.下列操作中正确的是( )
A、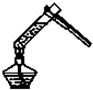 |
B、 |
C、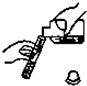 |
D、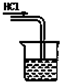 |
常温下,对pH=10的NaHCO3溶液中,各微粒的物质的量浓度分析正确的是( )
| A、c(CO32-)>c(H2CO3) |
| B、c(Na+)>c(HCO3-)>c(H+)>c(OH-) |
| C、c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D、c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
 如图所示,常温下电解5min后,Cu电极质量增加2.16g.
如图所示,常温下电解5min后,Cu电极质量增加2.16g. 的名称是
的名称是