题目内容
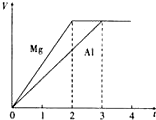 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.反应中镁和铝的( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.反应中镁和铝的( )| A、物质的量之比为3:2 |
| B、质量之比为3:2 |
| C、摩尔质量之比为2:3 |
| D、单位时间内生成H2的体积之比为2:3 |
考点:铝的化学性质,镁的化学性质,有关混合物反应的计算
专题:
分析:根据图象可知,两种金属得到的氢气一样多,然后根据金属镁、铝和足量的稀硫酸反应的化学方程式:Mg+H2SO4=MgSO4+H2↑,2Al+3H2SO4=Al2(SO4)3+3H2↑,即可找出各个量之间的关系.
解答:
解:A、由于Mg~H2,2Al~3H2,且两种金属得到的氢气一样多,因此镁和铝的物质的量的比是1:
=3:2,故A正确;
B、由于Mg~H2,2Al~3H2,且两种金属得到的氢气一样多,因此镁和铝的物质的量的比是1:
=3:2,则它们的质量的比为(3×24):(2×27)=4:3,故B错误;
C、镁和铝的摩尔质量之比和该化学反应毫无关系,即它们的摩尔质量之比为24:27=8:9,故C错误;
D、根据图象可知,单位时间内生成H2的体积之比为
:
=3:2,故D错误;
故选A.
| 2 |
| 3 |
B、由于Mg~H2,2Al~3H2,且两种金属得到的氢气一样多,因此镁和铝的物质的量的比是1:
| 2 |
| 3 |
C、镁和铝的摩尔质量之比和该化学反应毫无关系,即它们的摩尔质量之比为24:27=8:9,故C错误;
D、根据图象可知,单位时间内生成H2的体积之比为
| 1 |
| 2 |
| 1 |
| 3 |
故选A.
点评:本题以图象形式考查混合物计算、金属与酸的反应,难度不大,注意根据化学方程式进行有关的计算.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
下列关于有机化合物的认识正确的是( )
| A、淀粉和纤维素是同分异构体 |
| B、淀粉、蛋白质、油脂都属于天然高分子化合物 |
| C、植物油不能使溴的四氯化碳溶液褪色 |
| D、油脂在酸性条件下水解与在碱性条件下水解,产物不同 |
下列各组物质互为同系物的是( )
| A、CH4和C2H6 |
| B、CH3CH2CH2CH3和CH(CH3)3 |
| C、金刚石和石墨 |
| D、16O和18O |
下列中的实验一定不会出现沉淀现象的是( )
| A、CO2气体通入NaAlO2溶液中 |
| B、SO2气体通入BaCl2溶液中 |
| C、CO2气体通入饱和Na2CO3溶液中 |
| D、SO2气体通入Ba(OH)2溶液中 |
下列说法中正确的是( )
| A、在蔗糖中加入浓H2SO4后出现发黑现象,说明浓硫酸具有吸水性 |
| B、浓硝酸保存在棕色的细口瓶中,并置于低温阴暗处 |
| C、金属钠着火燃烧时,可用泡沫灭火器灭火 |
| D、正常雨水pH等于7,酸雨的pH小于7 |