题目内容
11.按照碳的骨架分类,下列叙述不正确的是( )| A. | 碳原子的骨架分类方法一般用于烃的分类 | |
| B. | 五个碳原子的环状化合物肯定是脂环化合物 | |
| C. | 不含苯环的碳环化合物都属于脂环化合物 | |
| D. | 芳香化合物就是指苯及苯的同系物 |
分析 A.按照碳的骨架分类,有机物可分为链状化合物和环状化合物,主要用于不含官能团的有机物;
B.根据苯环中至少含有6个C进行判断;
C.根据环状化合物分为脂环化合物和芳香化合物分析;
D.含有苯环的化合物属于芳香化合物,苯及苯的同系物属于芳香烃.
解答 解:A.烃分子中不含官能团,则其分类主要依据碳的骨架分类,故A正确;
B.五个碳原子的环状化合物,用于一定不含苯环,则该有机物肯定是脂环化合物,故B正确;
C.环状化合物分为脂环化合物和芳香化合物分析,则不含苯环的碳环化合物都属于脂环化合物,故C正确;
D.芳香化合物不一定为苯及其同系物,只要分子中含有苯环的化合物都属于芳香化合物,故D错误;
故选D.
点评 本题考查了常见有机物组成及分类方法判断,题目难度不大,明确常见有机物组成、结构及分类方法为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
1.生活中为了延长鲜花的寿命,通常会在花瓶中加入“鲜花保鲜剂”.下表是0.5L某种“鲜花保鲜剂”中含有的成分及含量.
请回答下列问题:
(1)“鲜花保鲜剂”中K+的物质的量浓度表示为$\frac{\frac{0.25g}{158g/mol}+\frac{0.25g}{174g/mol}×2}{0.5L}$(写出表达式即可,不需要化简)
(2)为了研究不同浓度的“鲜花保鲜剂”的保鲜功效,需配制多份不同物质的量浓度的
溶液进行研究.现欲配制480mL某物质的量浓度的“鲜花保鲜剂”,所需的玻璃仪器有:烧杯、玻璃棒、胶头滴管、500mL容量瓶.
(3)配制上述“鲜花保鲜剂”时,其正确的操作顺序是(每个操作只用一次):G→B→C→A→F→E→D.
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.在烧杯中加入适量水溶解
C.将烧杯中的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀,装入贴有标签的试剂瓶
E.改用胶头滴管加水,使溶液的凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
G.用电子天平称量各组成成分,并把它们放入烧杯中混合
(4)在溶液配制过程中,下列操作使溶液浓度偏小的是:AD.
A.定容时仰视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的“鲜花保鲜剂”而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,再用胶头滴管加水至刻度线.
| 成分 | 质量(g) | 摩尔质量(g/mol) |
| 蔗糖(C12H22O11) | 25.00 | 342 |
| 硫酸钾 | 0.25 | 174 |
| 阿司匹林(C9H8O4) | 0.17 | 180 |
| 高锰酸钾 | 0.25 | 158 |
| 硝酸银 | 0.02 | 170 |
(1)“鲜花保鲜剂”中K+的物质的量浓度表示为$\frac{\frac{0.25g}{158g/mol}+\frac{0.25g}{174g/mol}×2}{0.5L}$(写出表达式即可,不需要化简)
(2)为了研究不同浓度的“鲜花保鲜剂”的保鲜功效,需配制多份不同物质的量浓度的
溶液进行研究.现欲配制480mL某物质的量浓度的“鲜花保鲜剂”,所需的玻璃仪器有:烧杯、玻璃棒、胶头滴管、500mL容量瓶.
(3)配制上述“鲜花保鲜剂”时,其正确的操作顺序是(每个操作只用一次):G→B→C→A→F→E→D.
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.在烧杯中加入适量水溶解
C.将烧杯中的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀,装入贴有标签的试剂瓶
E.改用胶头滴管加水,使溶液的凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
G.用电子天平称量各组成成分,并把它们放入烧杯中混合
(4)在溶液配制过程中,下列操作使溶液浓度偏小的是:AD.
A.定容时仰视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的“鲜花保鲜剂”而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,再用胶头滴管加水至刻度线.
2.雾霾天气影响着我们的身体健康.下列有关空气污染的说法中,不正确的是( )
| A. | 酸雨的pH<5.6 | |
| B. | SO2、NO2都能引起酸雨 | |
| C. | 雾霾一定是由汽车尾气引起的 | |
| D. | 空气中的SO2主要来自煤、石油的燃烧 |
19.运用相关化学知识进行判断,下列结论错误的是( )
| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | NH4F 水溶液中含有 HF,因此 NH4F 溶液不能存放于玻璃试剂瓶中 | |
| C. | 可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 | |
| D. | 增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成 H2 的速率 |
16.下列属于氧化还原反应的是( )
| A. | CuO+2HCl═CuCl2+H2O | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | Zn+CuSO4═ZnSO4+Cu | D. | Ca(OH)2+CO2═CaCO3↓+H2O |
6.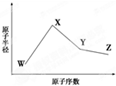 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
Ⅰ.(1)X位于元素周期表中的位置第三周期第ⅠA族;W的基态原子核外有2个未成对电子.
(2)X的单质和Y的单质相比,熔点较高的是Si(写化学式);Z的气态氢化物和溴化氢相比,较稳定的是HCl(写化学式).
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是SiCl4+4H2O=H4SiO4↓+4HCl.
Ⅱ.部分化学键的键能见下表:
(1)比较下列两组物质的熔点高低(填“>”“<”)SiC>Si SiCl4< SiO2
(2)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g),计算该反应的反应热△H=+236kJ•mol-1.
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.Ⅰ.(1)X位于元素周期表中的位置第三周期第ⅠA族;W的基态原子核外有2个未成对电子.
(2)X的单质和Y的单质相比,熔点较高的是Si(写化学式);Z的气态氢化物和溴化氢相比,较稳定的是HCl(写化学式).
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是SiCl4+4H2O=H4SiO4↓+4HCl.
Ⅱ.部分化学键的键能见下表:
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/ kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
(2)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g),计算该反应的反应热△H=+236kJ•mol-1.
3.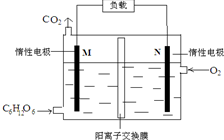 一种新型污水处理装置模拟细胞内生物电的产生过程,可将酸性有机废水的化学能直接转化为电能,下列说法中不正确的是( )
一种新型污水处理装置模拟细胞内生物电的产生过程,可将酸性有机废水的化学能直接转化为电能,下列说法中不正确的是( )
 一种新型污水处理装置模拟细胞内生物电的产生过程,可将酸性有机废水的化学能直接转化为电能,下列说法中不正确的是( )
一种新型污水处理装置模拟细胞内生物电的产生过程,可将酸性有机废水的化学能直接转化为电能,下列说法中不正确的是( )| A. | 与等量的C6H12O6完全燃烧放热比较,该装置发电效率高 | |
| B. | 若用该电池电解氧化铝制铝,与N极相连的电极有气体生成 | |
| C. | 电子流向:M→负载→N→电解质溶液→M | |
| D. | 当N极消耗5.6L(标况下)气体时,最多有NA个H+通过阳离子交换膜 |